Визначення валентності за формулами бінарних сполук
1. Яку валентність проявляють: 1) Сульфур у сполуці SO3; 2) Купрум у сполуці Сu2O; 3) Карбон у сполуці CO2; 4) Ферум у сполуці FeO; 5) Фосфор у сполуці P2O5?
2. Яка валентність Нітрогену, Фосфору, Хлору, Силіцію і Сульфуру у сполуках, що мають формули: NH3, PH3, HCl, SiH4, H2S?
3. Яка валентність елементів у сполуках, що мають такі формули: ZnS, Cu2S, Al2S3, SnS2, P2S5?
4. Визначити валентність кожного елемента в сполуках, що мають такі формули: Al2O3, HBr, Mn2O7, PbO2, CH4.
5. Визначити валентність елемента, що сполучений з Гідрогеном або Оксисеном, і записати її над символом елемента: CH4, P2O3, NO2, Cl2O, PbO, FeO, SO3, SiH4, CO, CO2, BaO.
6. Визначити валентність елемента, що сполучений з Гідрогеном або Оксисеном, і записати її над символом елемента: Al2O3, H2S, SO2, Na2O, NH3, CuO, Cr2O3, ZnO, HCl.
7. Визначити валентність елемента, що сполучений з Гідрогеном або Оксисеном, і записати її над символом елемента: MgO, P2O5, SiO2, K2O, HBr, Fe2O3, Ag2O.
12. Написати формули сполук Na, Cu(I), Cu(II), P(V), Ca(II), Fe(II), Fe(III), C(IV): а) з Оксигеном; б) з Хлором (I).
13. Написати форули сполук з Оксигеном таких елементів: N(V), C(II), C(IV), P(III), Si)IV), Ag(I), Zn(II), Al(III).
14.Складіть формули речовин, які містять такі елементи: 1) Алюміній й Оксиген; 2) Кальцій й Хлор (I); 3) Карбон (IV) й Гідроген; 4) Нітроген (III) й Оксиген; 5) Цинк й Бром (I); 6) Аюміній й Хлор (I); 7) Фосфор (V) й Оксиген; Магній і Нітроген (III); 9) Калій і Сульфур (II); 10) Фосфор (III) й Оксиген.
Дано:
ω(NH₄Cl) = 16%
ρ(р-ра NH₄Cl) = 1,148 гр/см³
----------------------------------------
Найти:
1) Для начала мы найдем массу раствора хлорида аммония:
Допустим у нас имеется 100 мл (100 см³ или 0,1 л) данного раствора, тогда:
m(р-ра NH₄Cl) = ρ(р-ра NH₄Cl) × V(р-ра NH₄Cl) = 1,148 гр/см³ × 100 см³ = 114,8 гр
2) Далее находим массу чистого вещества хлорида аммония по такой формуле:
m(NH₄Cl) = m(р-ра NH₄Cl) × ω(NH₄Cl)/100% = 114,8 гр × 16%/100% = 114,8 гр × 0,16 = 18,368 гр ≈ 18,37 гр
3) Далее находим молекулярную массу хлорида аммония:
M(NH₄Cl) = 14+1×4+35,5 = 14+4+35,5 = 53,5 гр/моль
4) Теперь находим количество вещества хлорида аммония:
n(NH₄Cl) = m(NH₄Cl)/M(NH₄Cl) = 18,37 гр / 53,5 гр/моль ≈ 0,34 моль
5) Теперь находим молярную концентрацию хлорида аммония:
ответ: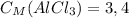 моль/л
моль/л