Na2S=2Na+S
S + O2=SO2
SO2 + O3=SO3 + O2
SO3 + H2O = H2SO4
H2SO4 + BaCl2 = BaSO4 + 2HCl
ответ:Дано:
m (Ba) = 10 г
Найти:
V (газа) - ?
Решение:
1) Написать уравнение химической реакции:
Ba + 2H2O => Ba(OH)2 + H2 ↑;
2) Вычислить молярную массу Ba:
M (Ba) = Ar (Ba) = 137 г/моль;
3) Вычислить количество вещества Ba:
n (Ba) = m (Ba) / M (Ba) = 10 / 137 = 0,07 моль;
4) Определить количество вещества H2 (учитывая коэффициенты в уравнении реакции):
n (H2) = n (Ba) = 0,07 моль;
5) Вычислить объем H2 (при нормальных условиях):
V (H2) = n (H2) * Vm = 0,07 * 22,4 = 1,6 л.
ответ: Объем H2 составляет 1,6 л.
Объяснение:
вроде так
Объяснение:
Fe₃O₄ (т.) + H₂ (г.) = 3 FeO (т.) + H₂O (г.) + Q
Q-?
Теплота реакции Q равна изменению энтальпии ΔH, взятому с обратным знаком: Q = - ΔH.
Будем считать, что реакция проводится при стандартных условиях.
Q = - ΔH = - ΔH°
Тогда для расчетов можно использовать стандартные энтальпии образования из справочников.
Стандартные энтальпии образования:
ΔH°f(H₂O, г.) = - 242 кДж/моль
ΔH°f(Fe₃O₄, т.) = -1117 кДж/моль
ΔH°f(FeO, т.) = - 265 кДж/моль
ΔH°f(H₂, г.) =0
Энтальпии образования элементов в стандартном состоянии равны нулю.
Изменение энтальпии химической реакции можно рассчитать как разность суммы энтальпий образования продуктов и суммы энтальпий образования реагентов (с учетом коэффициентов):
ΔH° = ∑ (ΔH°f (продукты)) - ∑ (ΔH°f (реагенты))
ΔH° = 3*ΔH°f(FeO, т.) + ΔH°f(H₂O, г.) - ΔH°f(Fe₃O₄, т.) - ΔH°f(H₂, г.) =
= 3*(-265) + (-242) - (-1117) - 0 = 80 кДж/моль
ΔH° > 0, то есть идет с поглощением теплоты, реакция эндотермическая.
Возвращаемся к тепловому эффекту реакции:
Q = - ΔH = - ΔH° = - 80 кДж/моль
ответ: - 80 кДж/моль
2)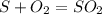
3)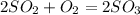
4)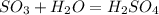
5)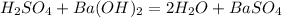 -стрелка вниз
-стрелка вниз