х г 4 г
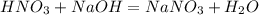
63 г 40 г
1. Сначала найдем чистую массу кислоты которая ушла на нейтрализацию 4 г гидроксида:
для полного взаимодействия 63 г кислоты необходимо 40 г гидроксида, а
для -- // -- х г____________________4 г, откуда
х=63*4/40=6,3 г
2. Теперь эту массу отнесем к массе всего раствора,которая дается по условиям задачи и равна 200 г(поэтому в дано запиши правильно:m(раствора)=200 г):
w(HNO3)=m(HNO3)/m(раствора)=6,3/200=0,03 или 3%
Например: Na3PO4 + CaCl2 = Ca3(PO4)2 + NaCl
Сразу обратите внимание, что у фосфат-иона (РО4) в правой части уравнения индекс равен двум. Поэтому, чтобы уравнять количества атомов фосфора и кислорода в левой и правой части, перед формулой молекулы фосфата натрия надо поставить коэффициент 2. Получится: 2Na3PO4 + СaCl2 = Ca3(PO4)2 + NaCl
Уравнивайте количество атомов натрия, приписав коэффициент 6 к молекуле хлористого натрия. Получается: 2Na3(PO4)2 + CaCl2 = Ca3(PO4)2 + 6NaCl
Осталось уравнять последние два элемента. Вы видите, что в левой части 1 атом кальция и 2 атома хлора, а в правой - 3 атома кальция и 6 атомов хлора. То есть, ровно в три раза больше! Подставляя коэффициент 3 к молекуле хлористого кальция, получите итоговое уравнение:
2Na3(PO4)2 + 3CaCl2 = Ca3(PO4)2 + 6NaCl