2Al+3O2=2Al2O3 Al(+3) O(-2) Al является восстановителем, O2 является окислителем.
2Al+6HCl=2AlCl3+3H2 Al(+3) Cl(-1)HCl является окислителем, Al является восстановителем.
2Fe+3Cl2= 2FeCl3 Fe(+3) Cl(-1) Cl2 является окислителем, Fe является восстановителем
Zn+2HNO3=Zn(NO3)2+H2 H(+1)N(+5)O(-2). Zn(+2)N(+5)O(-2) Zn является восстановителем, HNO3 является окислителем.
4Mg+5H2SO4= 4MgSO4+H2S+4H2O H(+1)S(+7)O(-2). Mg(+2)S(+7)O(-2). H(+1)S(-2). H(+1)O(-2) H2SO4 является окислителем, Mg является восстановителем.
Объяснение:
в простих сполуках ступінь окиснення 0
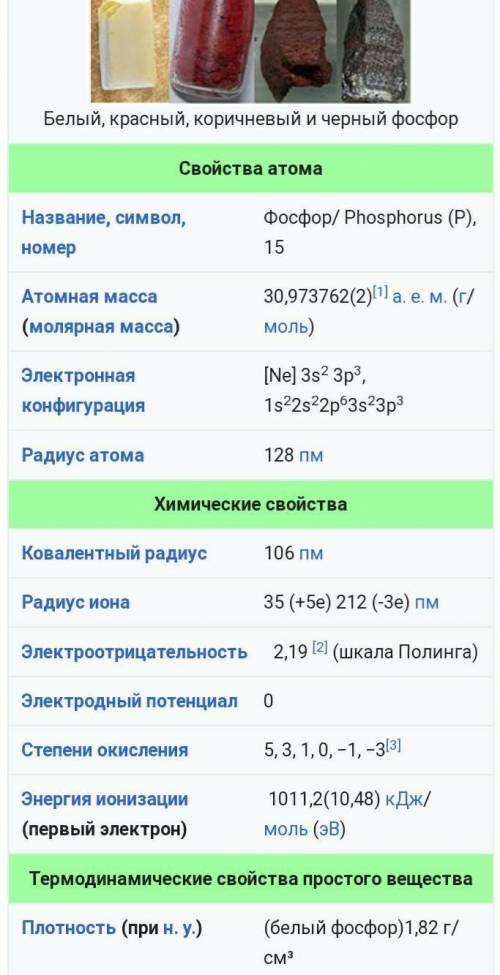
Фо́сфор (от др.-греч. φῶς — свет и φέρω — несу; φωσφόρος — светоносный; лат. Phosphorus) — химический элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) третьего периода периодической системы Д. И. Менделеева; имеет атомный номер 15. Элемент входит в группу пниктогенов. Фосфор — один из распространённых элементов земной коры: его содержание составляет 0,08—0,09 % её массы. Концентрация в морской воде 0,07 мг/л. В свободном состоянии не встречается из-за высокой химической активности. Образует около 190 минералов, важнейшими из которых являются апатит Ca5(PO4)3 (F,Cl,OH), фосфорит (Сa3(PO4)2) и другие. Фосфор входит в состав важнейших биологических соединений — фосфолипидов. Содержится в животных тканях, входит в состав белков и других важнейших органических соединений (АТФ, ДНК), является элементом жизни.
Объяснение:
1) 24 г Х г
2NaOH + FeSO4 = Fe(OH)2 + Na2SO4
n=2 моль n=1 моль
М = 40 г/моль М = 90 г/моль
m=80 г m=90 г
24 г NaOH - Х г Fe(OH)2
80 г NaOH - 90 г Fe(OH)2
m(Fe(OH)2 = 24 * 90 / 80 = 27 г
56 л Х г
2) 2 H2 + O2 = 2H2O
n=2 моль n=2 моль
Vm=22,4 л/моль М = 18 г/моль
V = 44,8 л m=36 г
56 л Н2 - Х г Н2О
44,8 л Н2 - 36 г Н2О
m(H2O) = 56 * 36 / 44,8 = 45 г