Для выражения частиц содержащихся, в определенной массе или объеме вещества, введено понятие количества вещества. Единицей количества вещества является моль. 1 моль-такое количество вещества, в котором содержиться 6,02* 10 в 23 степени частиц(атомов, молекул. ионов)
Na - постоянное авогадро равно 6,02*10 в 23 степени частиц.
Ню -число моль показывет взаимодействие числа моль и кол-ва частиц
Молярная масса численно равна относительной молярной массе
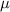 (мю)=m(вещ-ва)/ню
(мю)=m(вещ-ва)/ню
Пример:
Массу угарного газа возьмем 28 г
Ню(CO)=m/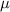 =28/28=1 моль
=28/28=1 моль
1) а) Ca-CaO-Ca(OH)2
2Са + О2 = 2СаО
СаО + Н2О = Са(ОН)2
б) Se-SeO2-H2SeO3
Se + O2 = SeO2
H2O + SeO2 = H2SeO3
2)
Дано: m(H2O) = 6 г
Найти: V(SO2) - ?
х моль 0,33 моль
SO2 + H2O = H2SO3
1моль 1 моль
n = m/M
M(H2O) = 18 г/моль
n(H2O) = 6 г / 18 г/моль = 0,33 моль
n(H2O) = n(SO2) = 0,33 моль
V = n*Vm
V(SO2) = 0,33 моль * 22,4 дм3/моль = 7,392 дм3
ответ: 7,392 дм3 (или 7,392 л)
3)
Дано: n(Na) = 0,1 моль
Найти: m(NaOH) -?
0,1 моль х моль
4Na + O2 = 2Na2O
4 моль 2 моль
0,1 = х
4 2
х = 0,05
n(Na2O) = 0,05 моль
0,05 моль х моль
Na2O + H2O = 2NaOH
1 моль 2 моль
0,05 = х
1 2
х = 0,1
n(NaOH) = 1 моль
m = n*M
M(NaOH) = 23 + 16 + 1 = 40 г/моль
m(NaOH) = 1 моль * 40 г/моль = 40 г
ответ: 40 г
5)
Объяснение:
СH2 = СH - СH(CH3) - СH3 + H2 -> CH3-CH2-CH(CH3)-CH3