1.Оксиды: CO2 оксид углерода (IV) или же углекислый газ, SO3 оксид серы (VI) или же серный газ, Na2O оксид натрия
Основания: KOH гидроксид калия, NaOH гидроксид натрия, Ca(OH)2 гидроксид кальция,
Кислоты: H2CO3 угольная кислота, HNO3 азотная кислота, H2SO4 серная кислота, HCl соляная кислота, H2SiO3 кремниевая кислота, H3PO4 фосфорная кислота, HBr бромоводородная кислота
Соли: K2CO3 карбонат калия, NaNO3 нитрат натрия, CaCl2 хлорид кальция, K3PO4 фосфат калия
2. 1) 2Al+3H2SO4=Al2(SO4)3+3H2
2)BaO+H2SO4=BaSO4+H2O
3) 3Ba(OH)2+2H3PO4=Ba3(PO4)2+6H2O
4) Na2SiO3+2HCl=2NaCl+H2SiO3
5) 2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O
6) 6NaOH+Al2(SO4)3=2Al(OH)3+3Na2SO4
7) FeCl3+3AgNO3=2AgCl+Fe(NO3)3
8) 2Al+3CuSO4=Al2(SO4)3+3Cu
9) CaO+CO=Ca+CO2
10) Na2O+H2O=2NaOH
118,5 г у г
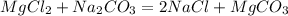
95 г 106 г
1. Найдем сначала чистую массу хлорида магния,так сказать, в растворе объемом 500 л:
если в 1 л жесткой воды содержится 237 мг хлорида, то
в 500 л______________________х г, откуда
х=500*237/1=118 500 мг или 118,5 г
2. Теперь подставив эту массу в уравнение,определим массу соды для полного осаждения ионов Магния:
для полного взаимодействия 95 г хлорида необходимо 106 г соды, а
для -- // -- 118,5 г_________________у г, откуда
у=118,5*106/95=132 г
Объяснение:
Дано:
Q=762кДж.
n(Fe)=1моль
m(Fe₂O₃)=100г.
Q₂-?
1. Определим молярную массу оксида железа(lll):
M(Fe₂O₃)=56х2+16х3=112+48=160г./моль
2. Определим количество вещества оксида железа(lll) в 100г.:
n(Fe₂O₃)=m(Fe₂O₃)÷M(Fe₂O₃)=100г.÷ 160г./моль=0,6моль
3. Запишем уравнение реакции:
Fe₂O₃ + 2Al = 2Fe + Al₂O₃
по уравнению реакции:
n(Fe₂O₃)=1моль n(Fe)=2моль Q-1524кДж.
по условию задачи:
n₁(Fe₂O₃)=0,6моль n₁(Fe)=1,2моль Q₁-X
4. Определим теплоту 1,2моль восстановления железа из оксида железа(lll) :
1моль Fe образуется 762 кДж.
1,2моль Fe образуется Х кДж.
Х кДж=1,2моль×762 кДж÷1моль =914,4кДж.
5. ответ: при восстановлении железа из 100 г. оксида железа(lll), методом алюминотермии, образуется 914,4кДж.