у г 25 г
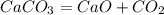
100 г 56 г
1. Сначала найдем теоретически возможный выход извести:
20 г извести - это только 80% от теоретически возможного, а
х г__________________100 г, откуда х=20*100/80=25 г
2. Подставив эту массу в уравнение реакции,найдем истинную массу карбоната,который прокалили:
при прокаливании 100 г карбоната образуется 56 г извести, а
при --//--//-- у г___________________25 г, откуда у=100*25/56=приблизительно 45 г
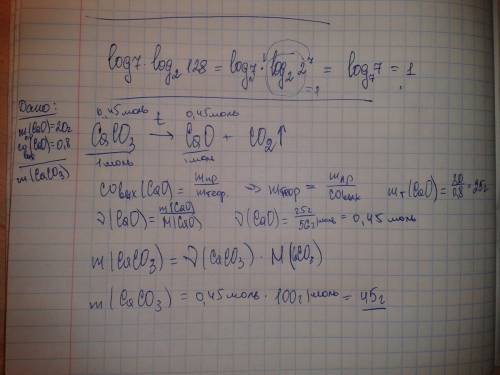
1) а)3,б)1,в)5,г)2,д)4
2)б
4)C4H9OH+CH3OH=?
C5H11COH+AgO=C5H11COOH+Ag (пентанавая к-та)
С2Н5СООН+Na=C2H5COONa+H2 (этанолят натрия)
С6H1206 (дрожжи)=2С2Н5ОН+2СО2 (этиловый спирт)