Задание 1.
Названия бинарных соеденинений:
Ca3N2 - нитрид кальция;
Al4C3 - карбид алюминия;
CaH2 - гидрид кальция;
FeO - оксид железа (||);
K2S - сульфид кальция;
MgCl2 - хлорид магния;
Na3P - фосфид натрия;
PH3 - фосфин или фосфид водорода.
Степени окисления:
Ca(+2)N(-3)
Al(-3)C(+4)
Ca(+2)H(-1) - пример исключения, когда водород приобретает степень окисления -1
Fe(+2)O(-2) - тоже пример исключения (довольно частый), когда кислород приобретает степень окисления -2.
K(+1)S(-2)
Mg(+2)Cl(-2)
Na(+1)P(-3)
P(+3)H(-1)
Задание 2.
Дано: m(CO2)= 14(г)
Найти: V(CO2)=? (л)
Формулы
m=n*M
V=n*Vm
постоянная величина, которая нам всегда известна Vm=22,4 (л/моль)
1) n(CO2)= m(CO2) : M(CO2)= 14 (г) : (12+16*2) (г/моль) = 0,3 (моль)
2) V(CO2)= n(CO2) * Vm = 0,3 (моль) * 22,4 (л/моль) = 6,7 (л)
ответ: V(CO2)= 6,7 (л).
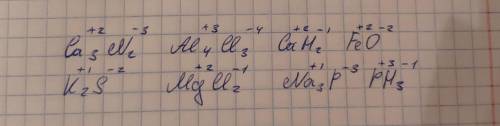
1. Просто вещество-это вещество состоящие из одного атома химического элемента примеры :Ca, O2, Mg
2. ZnO- оксид цинка, валентность цинка 2
MgO- оксид магния, валентность магния 2
SO2- оксид серы, валентность серы 4
P2O5- оксид фосфора, валентность фосфора 5
Al2O3 - оксид алюминия, валентность алюминия 3
Валентность у кислорода 2
3. 2Cu+O2=2CuO- соединение оксид меди
4P+5O2 =2P2O5 - соединение оксид фосфора
4. M(CaCO3) =40+12+16*3=100г/моль
W(Ca)=40:100=0,4 или 40%
W(C)=12:100=0,12 или 12%
W(O) =48:100= 0,48 или 48%
5. S+O2=SO2. 2Mg+O2=2MgO. 2H2S+3O2=2SO2+2H2O
6.Дано:
n(O2)=2,5моль
Найти:
m(O2)-?
V(O2)-?
N(O2)-?
Решение
m(O2) =n*M=2,5моль*32г/моль=80г
M(O2) =16*2=32г/моль
V(O2)=n*Vm=2,5моль*22,4л/моль=56л
N(O2)=n*NA=2,5моль*6*10^23=1,5*10^24
Металл - Магний (Mg) с молярной массой 24 г/моль
Объяснение:
Дано:
Так как по условию взят двухвалентный металл,
то уравнение реакции Ме и фосфора примет вид:
т.е. фосфид металла - вещество с формулой
Молярная масса фосфора
M(P) = 31 г/моль
Пусть, Me - некий металл с молярной массой х г/моль:
M(Me) = x г/моль.
Если исходная масса металла и масса его фосфида известны, можно вычислить массу фосфора, учавствовавшего в реакции:
Приведем известные нам данные в уравнении реакции:
Составим пропорцию (для бОльшего удобства вычислим пропорцию по Ме и Р)
М(Ме) = 24 г/моль
Следовательно,
искомый металл - магний: