ТЕКСТ МОЖЕТ БЫТЬ НЕ ПРАВИЛЬНЫМ ВСЕ НА ФОТО
Карточка индивидуальной работы по теме:
«СОЛИ»
7 класс
Выполните задания:
1. Напишите определение: соль – это
2. Запишите общую формулу соли. Как называются реакции по обнаружению частей соли?
3. Напишите формулы пяти солей соляной кислоты, пользуясь таблицей растворимости.
4. Можно ли распознать раствор поваренной соли индикатором?
5. Где встречаются соли в природе? Какие соли важны для организма человека?
6. Выпишите формулы солей и определите валентность металлов и кислотных остатков в
них:
Al2O3, H2SO4, Na2CO3, Cas, K2S, AlCl3, H20, CuSO4, Li2SO3, Ca(NO3)2, KClO4, CO2, FeCl2,
MnB, HCOONa, Al, Ba(OH)2, Вез (PO4)2, SO2, ZnS, Ca(OH)2, NO, Na2SiO3, S, H3PO4.
7. Заполните схему классификации солей:
Соли
По наличию H в составе
По количеству металлов
По растворимости
8. Работая с Таблицей растворимости веществ, запишите примеры для схемы.
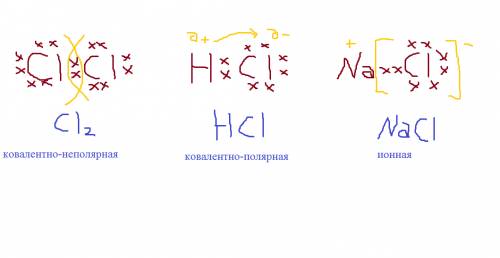
3. Из перечисленных химических элементов наименьшей
электроотрицательностью в соединениях обладает атом: Б. I.
4Положение элемента хлора в периодической системе:
Б. З-й период, главная подгруппа 7 группы.
5 Из перечисленных веществ наиболее ярко выраженные восстановительные свойства имеет:. Б. Иод.
6.Агрегатное состояние фтора при обычных условиях:
А. Газообразное.
7 . Химическая связь в молекуле иода:
Б. Ковалентная неполярная.
8. Пара формул веществ, в каждом из которых связь только ковалентная полярная: Б. НСI, HВг.
9. Название галогена, который был применен в боевых условиях как отравляющее вещество: Г. Хлор.
10.. Бром не взаимодействует с веществом, формула которого:
А. NаСI(р-р).
11 Приведите примеры соединений хлора, в которых он образует ковалентную неполярную, ковалентную полярную и ионную связь. ответ в приложении 1
14.NаCl +Н2sО4----NaHSО4 + НCl
Рассчитайте массу галогеноводорода, полученного из 1,5 молы иодида натрия. Может быть хлорида???
12. NаСI----Сl2---СuСl2 ---АgСl.
+1 -1 0 0
2NaCl = 2Na + Cl2 (электролиз)
2| Na⁺¹ +1e = Na⁰| восстанавливается
1| 2Cl⁻¹ -1 = Cl₂⁰ | окисляется
Сl2 + Cu = CuCl2
CuCl2 + 2AgNO3 = 2AgCl + Cu(NO3)2
Реакцию 1 рассмотрите с точки зрения ОВР.