I. сколько граммов 10% - ного раствора соляной кислоты нужно для нейтрализации 30 г 2% - ного раствегидроксида патрил? 12. скодъко граммов 20% - ного растрора сериой кислота нухно для нейтрализации 400 мл i i! раствора едного 13. сколько литров водорода при нормальных условиях получится при взаимодействии магния со 100 мл 201. неро раствора соляной кислоты, плотность рествора = 1, т/нд? 14. к 40 мл раствора серной кислоты ( р - 1,02 г/мл) прибавили 43,2 нд 7,4% - ного раствора едкото = 1,06 г/мл). найти процентную концентрацию раствора серной кислоты. 15. сколько миллилитров 30% - ного раствора серной кислоты = 1,07 г/мл) нужно взять для нейтрализации раствора щелочи, который содержит 16 г едкого натра?
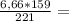 4,8г
4,8г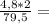 0,12г
0,12г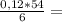 1,08г
1,08г
Соединение, формула которого CaCO3, очень заинтересовало меня, потому что, оно представлено бесконечным многообразием форм как в живой, так и неживой природе
Мне захотелось узнать, какие формы карбоната кальция встречаются в природе, какие химические превращения они претерпевают. Эти вопросы и определили содержание моего исследования.
Образование огромных пластов природного карбоната кальция, различных форм известняка, мела, мрамора, в первую очередь связано с жизнедеятельностью морских организмов: известковых водорослей, раковинных простейших, многих моллюсков, иглокожих, кораллов, корненожек. Они строят свой скелет из соединений кальция, преимущественно из карбоната — CaCO3. Наш родной город Москва стоит именно на таких отложениях, которые сформировались еще в каменноугольный период 300 миллионов лет тому назад.
Карбонат кальция (углекислый кальций) CaCO3, средняя соль угольной кислоты (H2CO3). В природе образует два минерала, различающиеся кристаллической структурой: широко распространённыйкальцит и арагонит.
Карбонат кальция трудно растворяется в воде (14 мг кальцита в 1 л при 18 °С), легко — в кислотах.
Природный карбонат кальция (известняк, мрамор) применяют как строительный материал; мел как наполнитель для резиновых смесей, бумаги, линолеума
— в производстве зубного порошка, косметических средств и т.д.
При нагревании выше 900 °С карбонат кальция разлагается:
Кальцит (известковый шпат) минерал, химического состава CaCO3.
Кальцит — один из наиболее распространённых минералов в земной коре, встречается особенно часто среди гидротермальных образований, в вулканических породах. Выпадает из известковых горячих источников в виде туфа (травертина). Огромные массы кальцита образуются в виде осадка в морских бассейнах, частично биогенным путём.
выбери