Так! Электролиты- это соединения, которые проводят электрический ток!
Сильные- те которые, почти необратимо диссоциируют в растворе, а слабые- незначительно диссоциируют в растворе. Т.е все электролиты, должны быть растворимы в воде, а иначе никак!
1) Ba(OH)2 - сильный электролит, а NH4OH - слабый.
Электролитическая диссоциация этих оснований:
Ba(OH)2 = Ba2+ + 2OH-;
NH4OH = NH4+ + OH-;
2) Mg(OO)2 - вообще не является электролитом, поскольку нерастворим, а Ca(OH)2 - слабым электролитом, так малорастворим, он диссоциирует на ионы незначительно:
Ca(OH)2 = Ca2+ + 2OH-
3) Тут всё ясно, и KOH и Ba(OH)2- сильные электролиты, они полностью диссоциируют в растворе:
KOH = K+ + OH-;
Ba(OH)2 = Ba2+ + 2OH-;
Значит, эти два основания являются сильными электролитами.
4) Как уже говорил, Mg(OH)2- неэлектролит, а вот NaOH- сильный, потому что растворим. Вот, как раз он и необратимо продиссоциирует на ионы:
NaOH = Na+ + OH-
ответ: 3.
Редактор формул не работает, поэтому коряво! Думаю, разберёшься, что к чему!
CH4 (г.) +2O2 (г.) =CO2 (г.) +2H2O (г.) +890 кДж
Так, нам известно, что в ходе данной реакции выделилось 890 кДж теплоты, т.е Q1= 890 кДж; Значит, реакция экзотермическая.
По уравнению реакции, найдём при каком объёме метана выделилось Q1:
Ведём рассчёты только по уравнению! Видно, что вступило в реакцию 1 моль 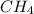 ,т.е n(
,т.е n(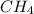 ) = 1 моль, значит объём прореагировавшего метана равен: V(
) = 1 моль, значит объём прореагировавшего метана равен: V(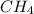 ) = Vm * n(
) = Vm * n(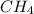 ) = 22,4 л/моль * 1 моль = 22,4 л.
) = 22,4 л/моль * 1 моль = 22,4 л.
Теперь нам известно, что при сгорании 22,4 л метана образовалось 890 кДж. А при сгорании 112 л метана количество теплоты неизвестно! Составим пропорцию:
22,4 л - 890кДЖ
112 л - x кДЖ => xкДж= 112 л * 890кДЖ/22,4 л= 4450 => при сгорании 112 л метана образовалось 4450 кДж теплоты, т.е Q2= 4450 кДж.
И проверь все рассчёты, а вдруг Не забудь тыкнуть на
Объяснение:
N₂ + O₂ = 2NO
объемов кислорода и азота 1:1
V(N₂):V(O₂)=22,4л. : 22,4л.