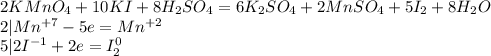
Объяснение:
Запишем уравнение:
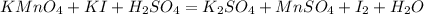
Расставим степени окисление и оставим их только у тех кто меняет их:
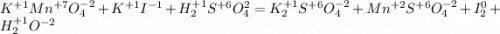
Останется:

Запишем ОВР редокс для марганца и йода:
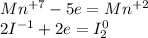
Перед йодом коэффициент 2, так как справа уже есть 2 йода, уравняем электроны:
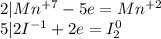
Перемножим коэффициенты:
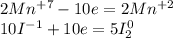
Mn - восстановитель, окисление
I - окислитель, восстановление
Расставим найденные коэффициенты:
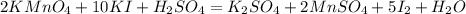
Продолжим уравнивать, слева калия 12, справа лишь 2, коэффициент 6 перед K₂SO₄:
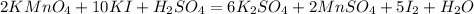
Справа сульфат остатков 8, а слева лишь 1, коэффициент 8 перед H₂SO₄:
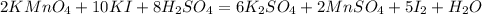
И наконец слева водорода 16, справа 2, коэффициент 8 перед водой:
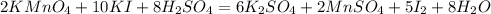
Уравнено!
ответ/відповідь: Г. 44,8
Дано:
m(BaCO₃) = 394 г
Найти/знайти:
V(CO₂) - ? (н.у.)
Объяснение/пояснення:
М(ВаСО₃) = 197 г/моль
Находим кол-во карбоната бария/знаходимо кількість барій карбонату:
n(BaCO₃) = m(BaCO₃)/M(BaCO₃) = 394 г/197 г/моль = 2 моль
Составляем УХР/складаємо РХР:
Ва(ОН)₂ + СО₂ = ВаСО₃ + Н₂О
Из УХР видно, что/з РХР бачимо, що n(CO₂) = n(BaCO₃)
n(CO₂) = 2 моль
Находим объем углекислого газа (н.у)/знаходимо об'єм вуглекислого газу (н.у):
V(CO₂) = n(CO₂)*Vm = 2 моль*22,4 л/моль = 44,8 л
ответ:/Відповідь: 44,8 л