Масса образовавшегося йода 50,8 г.
Объяснение:
Через раствор, содержащий 60 г иодида натрия, пропустили хлор объемом 15,6 л (н.у.). Определите массу образовавшегося йода.
Дано:
m(NaI) = 60 г;
V(Cl₂) = 15,6 л.
Найти: m(I₂).
Решение.
Более сильные галогены вытесняют более слабые из солей. Хлор вытесняет йод из солей.1) Запишем уравнения реакции между иодидом натрия и хлором, в результате которой образуется йод и хлорид натрия.
2NaI + Cl₂ → I₂ + 2NaCl
2) Найдем количество вещества иодида натрия, взятого для реакции.
M(NaCl) = 23 + 127 =150 г/моль.
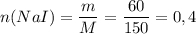 (моль)
(моль)
4) Найдем количество вещества хлора.
По закону Авогадро 1 моль любого газа занимает объем 22,4 л.
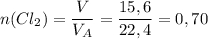 (моль).
(моль).
5) Определим количество выделившегося йода.
По уравнению реакции:
n(NaI) : n(Cl₂) = 2 : 1
У нас даны вещества в отношении
n(NaI) : n(Cl₂) = 0,4 : 0,7 = 2 : 3,5.
Иодид натрия в недостатке, по нему решаем задачу.
По уравнению реакции мольное отношение иодида натрия и йода:
n(NaI) : n(I₂) = 2 : 1 = 0,4 : 0,2.
В результате реакции выделится 0,2 моль йода.
6) Найдем массу выделившегося йода.
M(I₂) = 127 · 2 = 254 г/моль.
m(I₂) = n · M = 0,2 моль · 254 г/моль = 50,8 г.
Масса образовавшегося йода 50,8 г.
#SPJ1
Общая характеристика
Азот (символ N - от латинского Nitrogenium) - элемент 5 группы 2 периода (малый) периодической системы, порядковый номер 7, электронное строение атома 1s22s22p3. В соединениях проявляет степени окисления от -3 до +5.
Азот - неметалл, II период (малый) , V группа, главная подгруппа.
Атомная масса=14, заряд ядра - +7, число энергетических уровней=2
p=7, e=7,n=Ar-p=14-7=7.
N2O5 - кислотный оксид, летучее водородное соединение - NH3 оснОвного характера
Элемент азот имеет два стабильных изотопа: 14N и 15N.
Простое вещество молекулярный азот — достаточно инертный при нормальных условиях двухатомный газ без цвета, вкуса и запаха (формула N2), из которого на три четверти состоит земная атмосфера.
Б
Объяснение: