1.Восстановительные свойства металлов увеличиваются в ряду
1) Mg – Sr – Ca 3) Al – Mg – Be
2) Na – K – Rb 4) Mg – Na – Li
2. Наиболее активному металлу соответствует электронная конфигурация его атомов
1) 1s22s22p63s1 3) 1s22s22p63s23p1
2) 1s22s22p63s2 4) 1s22s22p63s23p64s1
3. Между собой не взаимодействуют
1) Zn и H2O 3) Ag и O2
2) Mg и HCl 4) Fe и AgNO3 (р-р)
4 . С соляной кислотой взаимодействует каждый из трех металлов группы
1) цинк, магний, серебро
2) железо, марганец, никель
3) алюминий, хром, медь
4) магний, висмут, ртуть
5. . Железо вытесняет металл из раствора соли
1) NiSO4 2) ZnCl2 3) Na2SO4 4) AlCl3
6. Водород выделяется в результате взаимодействия между
1) соляной кислотой и медью
2) цинком и раствором гидроксида натрия
3) золотом и концентрированной серношй кислотой
4) цинком и азотной кислотой
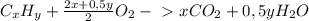

 г\моль
г\моль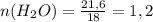 моль
моль
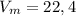 дм3\моль
дм3\моль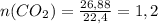 моль
моль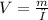
 дм3
дм3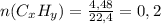 моль
моль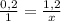
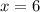
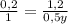


m'(Fe) = 100 г
ω(Fe) = 95.2% или 0,952
Найти:
m(FeS) - ?
1) Находим массу чистого железа (без примесей)
m(Fe) = m'(Fe)*ω(Fe)
m(Fe) = 100 г*0,952 = 95,2 г
2) Вычисляем количество вещества железа:
M(Fe) = 56 г/моль
n(Fe) = m(Fe)/M(Fe)
n(Fe) = 95,2 г/56 г/моль = 1,7 моль
3) Составляем уравнение реакции и по нем находим массу сульфида железа:
Fe + S = FeS
Из стехиометрических коэффициентов уравнения реакции следует, что n(FeS)=n(Fe) = 1,7 моль
M(FeS) = 88 г/моль
m(FeS) = n(FeS)*M(FeS)
m(FeS) = 1.7 моль*88 г/моль = 149,6 г
ответ: 149,6 г