Там много чего может получаться в зависимости от условий реакции. Во первых - самовоспламеняется в хлоре только белый фосфор и другие его молекулярные модификации. Красный фосфор в виду его полимерной и поэтому менее реакционно структуры в хлоре не самовоспламеняется, его надо подогревать. РСl5 твердое сильно дымящее на воздухе вещество, образуется при избытке хлора. А сначала образуется PCl3. Это жидкость, которая растворяет в себе PCl5,который реагирует с фосфором давая две молекуля PCl3,котрые потом доокисляются хлором до PCl5 и реагируют с новыми порциями фосфора и т. д. Таков механизм реакции. Напряму реакция с фосфором идет только в начале, и на практике ее стараются не делать так как при этом в колбе такой фейерверк что становится страшно. Просто в начале в колбу наливают немного PCl3 для затравки, потом уже пускают хлор. И еще, при попадании в реактор воды там образуется хлорокись фосфора POCl3 и хлороводород.
P.S. У тебя в уравнении формула хлора неправильная, должно быть Cl2,это даже по балансу видно-у тебя до реакции 5 атомов хлора а после реакции 10. Так не бывает, это только во время ядерных реакция появляютсмя новые атомы, а во время химических перегруппирововаются только уже существующие. Хлор в обычных условиях состоит из двухатомных молекул а не из атомов.
Я сам не мастер объяснять, и ошибки могут присутствовать. Перечитай несколько раз, чтобы быть уверенным что правильно\не правильно.
При взаимодействии двух оксидов, в данном случае, щелочного и кислотного, образуется соль! Реакция получила название - реакция соединения:
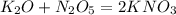 .
.
Качественный и количественный состав исходных веществ:
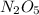 - оксид азота (V). Кач. состав: азот(N), кислород(O); Кол. состав: 2 атома азота(N), 5 атомов кислорода(O);
- оксид азота (V). Кач. состав: азот(N), кислород(O); Кол. состав: 2 атома азота(N), 5 атомов кислорода(O);
Качественный и количественный состав продукта реакции:
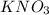 - соль; Кач. состав: калий, азот(N), кислород(O); Кол. состав: 1 атом калия, 1 атом азота(N), 3 атома кислорода(O). Всё!
- соль; Кач. состав: калий, азот(N), кислород(O); Кол. состав: 1 атом калия, 1 атом азота(N), 3 атома кислорода(O). Всё!
Кто проголосовал, все мои ошибки, которые здесь увидел в л.с! Или не**р просто так голосовать Если человек знает, чего он хочет, значит, он или много знает, или мало хочет."
1. 1 моль CaCI2 • 6 H2O Г 219 г
Объяснение:
У Вас допущены ошибки, уточните. Остальные массы не совпадают с предложенным выбором:
2. 5 моль СuSO4•5 H2O
m(СuSO4•5 H2O)=64+32+64+90=250х5=1250г.
3. 10 моль FeSO4•H2O m(FeSO4•H2O)=56+32+64+18=170х10=1700г.
4. 4.2 моль Zn( NO3)2•6H2O
m(Zn( NO3)2•6H2O)=65+124+108=297х4,2=1213,8г.
А 1250 г
Б 2780 г
В 594 г
Д 900 г