масса осадка равна 5,88г.
m[Cu(OH)₂]=5,88г.
Объяснение:
Дано:
m(CuSO₃)=8г.
m[Cu(OH)₂]-?
1. Определим молярную массу сульфита меди:
M(CuSO₃)=64+32+3x16=144г./моль
2. Определим количество вещества сульфита меди в 8г.:
n=m÷M
n₁(CuSO₃)=m(CuSO₃)÷M(CuSO₃)
n₁(CuSO₃)=8г.÷144г./моль=0,055моль (округлим)=0,06моль
3. Запишем уравнение реакции:
CuSO₃+2NaOH=Cu(OH₂)↓+Na₂SO₃
по уравнению реакции:
n(CuSO₃)=n[Cu(OH₂])=1моль
по условии задачи:
n₁(CuSO₃)= n₁[Cu(OH₂)]=0,06моль
n₁[Cu(OH)₂]=0,06моль
4.Определим молярную массу гидроксида меди:
M[Cu(OH)₂]=64+2x (16+1)=98г./моль
5. Определим массу осадка гидроксида меди(ll):
m[Cu(OH)₂]= n₁[Cu(OH)₂]xM[Cu(OH)₂]
m[Cu(OH)₂]=0,06мольх98г./моль=5,88г.
Уравнение реакции( один из вариантов):
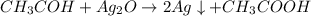
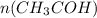 = 4,4 / 44= 0,1 моль
= 4,4 / 44= 0,1 моль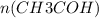 =
= 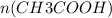 = 0,1 моль
= 0,1 моль
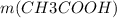 =
= 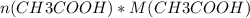 = 0,1 * 60 = 6 г.
= 0,1 * 60 = 6 г.
Чтобы расчитать выход продукта, нам нужно узнать сколько теоретически должно было выделиться продукта( "на бумаге").
Воспользуемся известной массой уксусного альдегида и найдём, сколько этого самого альдегида вступило в реакцию:
n( количество вещества) = m( масса) / M( молярная масса) - общая формула
Из уравнения реакции видно, что коэффициент перед уксусным альдегидом равен коэффициенту перед уксусной кислотой, т.е.
Теперь, пользуясь уже знакомой формулой n( количество вещества) = m( масса) / M( молярная масса), мы можем найти массу ( теоретическую) уксусной кислоты:
Выход продукта расчитываем по формуле:
w = m( практ) / m( теор) * 100% = 90%
ответ: выход продукта составил 90%.