Объяснение:
1) Жиры — органические вещества, продукты этерификации карбоновых кислот и трёхатомного спирта глицерина.
2) Глицерин.
3) В состав молекул жиров входят остатки высших карбоновых кислот: стеариновой C 17 H 35 COOH , пальмитиновой C 15 H 31 COOH , олеиновой C 17 H 33 COOH .
4) Да, это смесь сложных эфиров глицерина и высших жирных кислот (ВЖК)
5) Физико-химические и химические свойства жиров
6) При нагревании, кроме растительного оно и про комнатной температуре жидкое
7) Жидкие жиры растительного происхождения называются маслами и представляют собой сложные эфиры глицерина и высших непредельных кислот .
8) Все жиры животного происхождения - твёрдые вещества. Исключение лишь составляет рыбий жир
9) Жиры практически нерастворимы в воде, хорошо растворимы в органических растворителях
10)
11) Иодное число — масса иода (в г), присоединяющегося к 100 г органического вещества.
12) При омылении жиров
13) При длительном хранении под действием влаги, кислорода воз- духа, света и тепла непредельные жиры приобретают неприятный запах и вкус. Этот процесс называется прогорканием
14) Жидкие жиры можно перевести в твердые путем реакции гидрогенизации
15) С пищевым жиром организм получает жирорастворимые витамины А, Д, Е, К, незаменимые жирные кислоты, фосфатиды, холестерин, холин
16)
17) Жиры, также триглицериды, триацилглицериды
18) Это соли жирных кислот, обладающие моющими свойствами
19) В зависимости от того, какие соли (натриевые или калиевые) применяются при производстве, получается либо твёрдое мыло, либо жидкое
20)
Спирты: Метанол (CH3OH), Этиленгликоль (C2H6O2), Бутанол (C4H9OH), Глицерин (C3H8O3)
Альдегиды: Этаналь (C2H4O), Метаналь (HCHO), Пропаналь (СН3СН2СHO)
Карбоновые кислоты: Уксусная кислота (CH3COOH), Муравьиная кислота (HCOOH), Этановая кислота (CH3COOH)
Сложные эфиры: Метиловый эфир уксусной кислоты (CH3COOCH3)
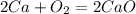
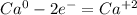 ·2 восстановитель полуреакция окисления
·2 восстановитель полуреакция окисления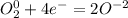 ·1 окислитель полуреакция восстановления
·1 окислитель полуреакция восстановления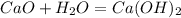
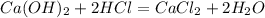
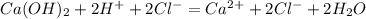
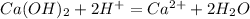
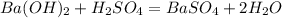
![m[Ba(OH)_2]=](/tpl/images/0276/7725/752a4.png) =50 · 0,18 = 9 г
=50 · 0,18 = 9 г![n[Ba(OH)_2]= \frac{m[Ba(OH)_2]}{M[Ba(OH)_2]} = \frac{9}{171} =0,0526](/tpl/images/0276/7725/43f28.png) моль
моль![n(BaSO_4)=n[Ba(OH)_2]=0,0526](/tpl/images/0276/7725/a4a1c.png) моль
моль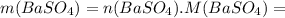 =0,0526 · 233=12,2558 г ≈12,26 г
=0,0526 · 233=12,2558 г ≈12,26 г
Базовый уровень
1.Заряд ядра и число электронов на внешнем уровне в атоме фтора соответственно равны:
4) 9 и 7
2.В ряду химических элементов Si—>А1—>Mg—>Na увеличивается:
отдавать электроны
3.Ковалентная неполярная связь существует в веществе:
2)Р4
4.В веществе, формула которого KNO2, степень окисления азота равна:
2)+3
5.Вещества, формулы которых Na2CO3 и А1(0Н)3, являются соответственно:
1)солью и амфотерным гидроксидом
6.Реакция между цинком и сульфатом меди (II) относится к реакциям:
3)замещения
7.Электрический ток проводит:
4)раствор хлорида натрия
8.Реакция возможна между растворами веществ:
2)AgNO3 + Nal
9.Реакция при комнатной температуре возможна между веществами:
1)натрием и кислородом
10.Верны ли утверждения? А) Водород следует собирать в пробирку, расположенную дном вверх; Б) Сероводород не ядовит:
1)верно только А
11.Общим для углерода и азота является:
2)число энергетических уровней
4)они образуют простые вещества — неметаллы
12.Для этанола верны следующие утверждения:
1)вещество содержит гидроксильную группу
4)вещество горит на воздухе
13. Установите соответствие между названием вещества и реагентами, с которыми это вещество может взаимодействовать.
НАЗВАНИЕ ВЕЩЕСТВА
А)SiO2 3)HF, NaOH
Б) раствор H2SO4 2)СаСО3, ВаС12
В)Na3PO4 2)СаСО3, ВаС12