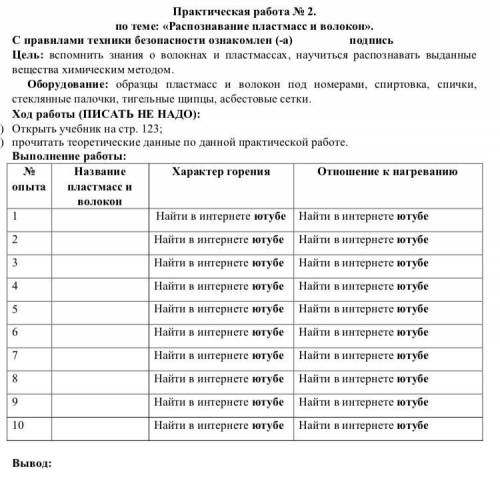
Zn + СuSO4 – ZnSO4 +Сu
65,4 г 63,5 г
по уравнению разница в массе составляет 65,4-63,5=1,9 г
Значит 63,5 г Сu даст разницу 1,9 г
а х г Сu даст разницу 0,2 г х=63,5*0,2/1,9=6,684 г
Сu осело на пластинку
n (Сu)= m/М=6,684/63,5=0,105 моль
n (СuSO4)= n (Сu)= 0,105 моль
m(СuSO4)= 0,105 моль*160=16,8 г
В исходном растворе содержалось 0,105 моль или 16,8 г СuSO4
Циклоалканы-галоненирование, нитрование, дегидрирование, горение, реагирует с активными металлами.
Алкены-реакция электрофильного присоединения, гидрирование, галогенирование, гидратация,окисление,изомеризация,полимеризация.
Алкины-гидрирование, галогенирование, гидрогалоненирование, гидратация, полимеризация, окисление.
Арены-галогенирование, нитрование, алкенирование, окисление.
Спирты- щелочной и щелочноземельный металл с образованием солей алкоголят, реакция этерификации ,аминирование,замещение, внутри молекулярная/межмолекулярная дегидратация, окисление.
Алкадиены-гидрирование, галогенирование, гидратация, гидрогалогенирование, полимеризация.
Альдегиды-гидрирование, гидратация, полимеризация, поликонденсация, окисление, альдольно-кротоновая конденсация.
Карбоновые кислоты-разлодение, этерификация, дегидратация, кислотный /щелочной гидролиз, гидрирование, окисление.
Сложные эфиры-кислотный/щелочной гидролиз, гидрирование, горение.