
Масса образовавшегося йода 50,8 г.
Объяснение:
Через раствор, содержащий 60 г иодида натрия, пропустили хлор объемом 15,6 л (н.у.). Определите массу образовавшегося йода.
Дано:
m(NaI) = 60 г;
V(Cl₂) = 15,6 л.
Найти: m(I₂).
Решение.
Более сильные галогены вытесняют более слабые из солей. Хлор вытесняет йод из солей.1) Запишем уравнения реакции между иодидом натрия и хлором, в результате которой образуется йод и хлорид натрия.
2NaI + Cl₂ → I₂ + 2NaCl
2) Найдем количество вещества иодида натрия, взятого для реакции.
M(NaCl) = 23 + 127 =150 г/моль.
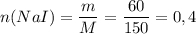 (моль)
(моль)
4) Найдем количество вещества хлора.
По закону Авогадро 1 моль любого газа занимает объем 22,4 л.
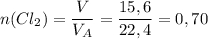 (моль).
(моль).
5) Определим количество выделившегося йода.
По уравнению реакции:
n(NaI) : n(Cl₂) = 2 : 1
У нас даны вещества в отношении
n(NaI) : n(Cl₂) = 0,4 : 0,7 = 2 : 3,5.
Иодид натрия в недостатке, по нему решаем задачу.
По уравнению реакции мольное отношение иодида натрия и йода:
n(NaI) : n(I₂) = 2 : 1 = 0,4 : 0,2.
В результате реакции выделится 0,2 моль йода.
6) Найдем массу выделившегося йода.
M(I₂) = 127 · 2 = 254 г/моль.
m(I₂) = n · M = 0,2 моль · 254 г/моль = 50,8 г.
Масса образовавшегося йода 50,8 г.
#SPJ1
2al+3cl2=2alcl3
alcl3+3naoh=3nacl+al(oh)3-белый осадок
al(oh)3+naoh={t°}naalo2+2h2o
2naalo2+4h2so4=na2so4+al2(so4)3+4h2o
al2(so4)3+6naoh=3na2so4+2al(oh)3-белый осадок