1 )оксид лития-Li2O
гидроксид натрия NaOH
Серная кислота - H2SO4
Оксид углерода - CO2
2 NaOH + H2SO4= Na2SO4 + 2 H2O
Li2O + H2SO4 = Li2SO4 + H2O
Li2O + CO2 = Li2CO3 ( при нагревании )
CO2 + 2 NaOH(избыток или расплав) = Na2CO3 + H2O
CO2(избыток) + NaOH = NaHCO3
2)
4 P+ 5 O2 = 2 P2O5 ( На самом деле: P4 (фосфор- белый) + 5 O2 = P4O10 P.S все немного сложнее) для общего развития реакция идет примерно так но в школе писать не советую, если интересно посмотрите )
P2O5 + H2O = H3PO4 ( опять же реакция для школьной химии )
3 KOH + H3PO4 = K3PO4 + 3 H2O
K3PO4 + Сa(OH)2 = Ca3(PO4)2↓ + KOH
Ca3(PO4)2 + 3 H2SO4 = 2 H3PO4 + 3 CaSO4
3)
фосфат алюминия- Al PO4
сульфид серебра - Ag2S
оксид марганца - MnO3
гидроксид магния Mn(OH)2
хлорид аммония NH4Cl
нитрат свинца (II) Pb (NO3)2
4)
a) Mg+ CuSO4 = MgSO4 + Cu
4 Mg + 5 H2SO4(концентрированная) = 4 MgSO4 + H2S↑ + 4 H2O
б) CaO+ H2O= Ca(OH)2
Ca(NO3)2 + KOH = KNO3 + Ca(OH)2↓
Ca + H3PO4 = Ca
5) 2AgNO3 + CuCl2 = 2AgCl↓ + Cu(NO3)2
Дано: Решение:
m(AgNO3) = 1,7 г n ( AgNO3) = m/M = 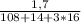 = 0,01 моль = n(AgCl)
= 0,01 моль = n(AgCl)
m ( AgCl) - ? m (AgCl)= n(AgCl) * M(AgCl)= 0,01 моль*
(108г/моль+35,5г/моль) = 1,435 г
ответ: 1,435 г
P.S. n- количество вещества ( еще обозначают как ν - "ню" )
6) CaO + H2SO4 = CaSO4 + H2O
Дано: n (CaO) - ?
m(H2SO4) = 14,7 г
n(H2SO4) = m/M = 14,7 г/ (2г/моль+32г/моль+4*16г/моль) = 0,15 моль=
= n(CaSO4)
m(CaSO4) = n*M = 0,15 моль*(40г/моль + 32г/моль+4*16г/моль)= 15,3 г
7)
Я не могу тут сделать нормальную таблицу, поэтому пусть это таблица : по горизонтали то что мы добавляем в пробирки по вертикали признаки реакции
----- | HNO3 | Ba(NO3)2
Na2CO3 | CO2↑ | помутнение воды
NaNO3 | -- | --
Na2SO4 | -- | осадок
Na2CO3 +2 HNO3 = H2O + CO2↑ + 2NaNO3
NaNO3 + HNO3 ≠
Na2SO4 + HNO3 ≠
Na2CO3 + Ba(NO3)2= BaCO3↓ + 2 NaNO3
Na2SO4 + Ba(NO3)2 = BaSO4↓ + 2 NaNO3
Объяснение:
Часть А. Выберите один правильный ответ.
А1. Четыре энергетических уровня содержит электронная оболочка атома:
а) калия
А2. Шесть электронов находятся на внешнем энергетическом уровне атома:
г) кислорода
А3. Ряд чисел 2,8,5 соответствует распределению электронов по энергетическим уровням атома: в) фосфора
А4. Наиболее ярко выражены неметаллические свойства у: г) C
А5. Выберите соединение с ковалентной полярной связью:
б) H2S
А6. Выберите формулу соединения серы, в котором она проявляет степень окисления -2:
в) MgS
А7. Выберите ряд формул, в котором все вещества являются основаниями:
в) КОН, Fe(OH)3, NaОН
А8. Выберите формулу оксида железа (III): в) Fe2O3
А9. Уравнение реакции замещения:
а) Zn + 2HCl = ZnCl2 + H2
А10.Оксид кальция реагирует с: а) HNO3
А11. В лаборатории кислород получают:
б) разложением перманганата калия
в) электролизом воды г) взаимодействием натрия с водой
А12. Какой объем при н.у. занимает 2 моль водорода Н2:
в) 44,8 л
А13. В каком ряду расположены азотная кислота, карбонат натрия, оксид фосфора (V):
б) HNO3, Na2 CO3, P2O5
А14. В каком ряду расположены только кислотные оксиды:
б) Р2O5, CO2, SO3
А15. Чему равна сумма коэффициентов в уравнении реакции:
Сa(OH)2 + 2HNO3 = Ca(NO3)2 + 2H2O б) 6
А16. Какое из веществ взаимодействует с серной кислотой:
б) алюминий
А17. Реакция взаимодействия серной кислоты и цинка относится к реакциям:
г) замещения
А18. К окислительно-восстановительным реакциям относится реакция между:
а) водородом и кислородом
А19. Какое количество вещества составляет 5,4 г воды:
г) 3 моль
А20. Чему равна масса 1,5 моль CО2 -- б) 66г.
Часть В.
В1. Ядро атома 15N содержит 7 протонов и 8 нейтронов.
В2. Расположите элементы в порядке усиления металлических свойств
г) Si б) Al а) Mg в) Na
В3. Установите соответствие между формулой вещества и его принадлежностью к определенному классу неорганических соединений.
Класс веществ: Формула вещества:
1) оксиды е) P2O5
2) основания д) Fe(OH)3
3) кислоты а) HNO2
4) средние соли г) Mg(NO3)2
б) NaHSO4 кислая соль
в) Mg(OH)NO3 основная соль
В4. Установите соответствие между реагентами и названием продуктов реакции
Реагенты Продукты реакции
1) BaCl2 + Na2SO4 д) сульфат бария и хлорид натрия
2) BaO + HCl а) хлорид бария и вода
3) Ba + H2O в) гидроксид бария и водород
4) Ba(OH)2 + HNO3 б) нитрат бария и вода
В5. Массовая доля кислорода в серной кислоте H2SO4 равна 65,3%
Часть С.
С1. Пронумеруйте реакции и запишите уравнения химических реакций, соответствующих схеме превращений:
Cu → CuO → CuCl2 → Cu(OH)2 → Cu SO4 → Cu
2Cu+O₂ = 2CuO
CuO+2HCI = CuCl₂+H₂O
CuCl₂+2NaOH = Cu(OH)₂↓+2NaCI
Cu(OH)₂+H₂SO₄ = CuSO₄+2H₂O
CuSO₄+Fe = Cu↓ +FeSO₄
С2. Вычислите массу оксида кальция, полученного при обжиге 250 г карбоната кальция.
Дано:
m(CaCO₃)=250г.
m(CaO)-?
1. Определим молярную массу карбоната кальция:
M(CaCO)₃=40+12+48=100г./моль
2. Определим количество вещества карбоната кальция в 250г.:
n₁(CaCO)₃)=m(CaCO₃)÷M(CaCO)₃=250г÷100г./моль=2,5моль
3. Запишем уравнение реакции:
CaCO₃=CaO+CO₂
а) по уравнению реакции количество вещества:
n(CaCO₃)=1моль n(CaO) =1моль
б) по условию задачи количество вещества:
n₁(CaCO₃)=2,5моль n₁(CaO) =2,5моль
4. Определим молярную массу оксида кальция :
M(CaO)=40+16=56г./моль
5. Определим массу количеством вещества 2,5моль:
m(CaO)= n₁(CaO)×M(CaO)=2,5моль×56г./моль=140г.
6. ответ: m(CaO)=140г.