Пропандиол 1,2
Объяснение:
Масса компонентов в углеводороде будет равна
С - (10,08/22,4)*12=5,4 H - (10.8/18)*2=1,2
В сумме 5,4+1,2=6,6, а исходник 11,4 значит он кислородосодержащее
Теперь находим процентное соотношение каждого компонента
С - (5,4/11,4*12)=0,0394
H - 1.2/11.4=0.105
O - (11.4-6.6)/(11.4*16)=0,0263
Находим общий делитель - 0,013
Теперь коэффициенты элементов
С - 0,0394/0,013=3
H - 0.105/0,013=8
O - 0.0263/0,013=2
C3H8O2 - это пропиленгликоль
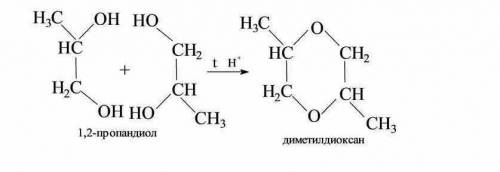
Межмолекулярная дегидратация на примере пропиленгликоля (пропандиола 1,2)
Натрий (Na):Физическое св-ва: Натрий-металл серебристо-белого цвета с ярко выраженным металлическим блеском, настолько мягкий, что легко режется ножом. Лёгкое и легкоплавкое вещество, имеет высокую теплопроводность и электропроводность. То есть, это типичный металл.
Химические св-ва:При горении на воздухе или в кислороде образуется пероксид натрия:2Na + O2 →to Na2O2.
Хлор (Cl):При нормальных условиях хлор — жёлто-зелёный газ с удушающим запахом.
Химические св-ва:На валентном уровне атома хлора содержится 1 неспаренный электрон: 1s2 2s2 2p6 3s2 3p5, поэтому валентность, равная 1 для атома хлора, очень стабильна. За счёт присутствия в атоме хлора незанятой орбитали d-подуровня атом хлора может проявлять и другие степени окисления.
нет, не прав
Объяснение:
в скобочках буду указывать степень окисления, которая будет наверху написана
Чтобы решить задачу, составим уравнения реакций
1. 2H(+)Cl(-) + K(+)2O(-2) = H(+)2O(-2) + 2K(+)C(-)l
Из уравнения видно, что ни у одного элемента степень окисления не изменилась, оттого это не ОВР
Также стоит сказать, что реакции обмена НИКОГДА не являются ОВР
2. Zn(2+) + 2H(+)Cl(-) = Zn(2+)Cl(-)2 + H(0)2
Степень окисления изменилась у водорода (была +, стала 0), поэтому это ОВР.
2H(+) -2e = H(0)2
Реакции замещения ВСЕГДА овр
3. 4Na(0) + O(0)2 = 2Na(+)2O(-)
У натрия и кислорода изменилась степень окисления, поэтому это ОВР
4Na(0)-4e = 2Na(+)2
O(0) + 1e = O (-)