ответ: 83,33%
Дано:
D'(He) (cм.) = 2,6
D"(Ne)(cм.) = 1,2
Найти:
η(СH₃OH)-?
Объяснение:
M(СH(=O)H) = 30 г/моль
М(Не) = 4 г/моль
М(Н₂) = 2 г/моль
M(Ne) = 20 г/моль
Примем кол-во муравьиного альдегида за х моль, а водорода за у моль, составим систему уравнений и решим ее:
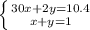
Решив систему получим: х=0,3; у=0,7
n(HCOOH) = 0,3 моль; n(H₂)=0,7 моль
НС(=О)Н + Н₂ ⇒ СН₃ОН
Из УХР n(НС(=О)Н):n(H₂) = 1:1, по расчетам исходя из условия задачи n(НС(=О)Н):n(H₂) = 0,3:0,7 = 3:7 = 1:2,33, то есть водород взят в избытке; n(теор. CH₃OH) = 0,3 моль - теоретический количественный выход
Исходя из УХР и расчетов, количество водорода осталось Δm(H₂)=0,7моль-0,3 моль = 0,4 моль
Молярная масса смеси после реакции (M'(см.) по неону:
M'(см.) = D"(Ne)(cм.)*M(Ne) = 1,2*20 г/моль = 24 г/моль
Примем количество непрореагировавшихся муравьиного альдегида и водорода за x'
30x' + 2x' = 24
32x' = 0,75
x'=0,75
Прореагировало 1 моль-0,75 моль = 0,25 моль
Практический количественный выход n(пр.СН₃ОН) = 0,25 моль
η(СH₃OH) = n(пр.СН₃ОН)/n(теор. CH₃OH)
η(СH₃OH) = 0,25 моль/0,3 моль = 0,8333 или 83,33%
ответ: 83,33%
Объяснение:
1. Молярная масса гелия 4г/моль, значит, средняя молярная масса исходной смеси равна 2,6*4 = 10,4 г/моль. Молярная масса муравьиного альдегида равна 30 г/моль, водорода - 2 г/моль. Мольное отношение газов в смеси равно (10,4 - 2)/(30 - 10,4) = 0,3:0,7. Следовательно, в смеси содержалось 0,3 моль муравьиного альдегида и 0,7 моль водорода.
2. Пропускание смеси над нагретым платиновым катализатором приводит к образованию метанола по уравнению
НСОН + Н2 ---> СН3-ОН
Соотношение между количествами веществ вступившего в реакцию муравьиного альдегида и образовавшегося метанола 1:1, значит, теоретический выход продукта реакции равен 0,3 моль.
Пусть образовалось х моль метанола. Тогда во взаимодействие вступило х моль альдегида (осталось (0,3 - х) моль) и х моль водорода (осталось (0,7 - х) моль).
А дальше нужно проверять условие. Если дана плотность по неону (М (Ne) = 20 г/моль), то средняя молярная масса смеси получается равной 1,2*20 = 24 г/моль, и она выше, чем до реакции, чего быть не может. Приведу окончание решения для плотности по тому же гелию, что и вначале.
Средняя молярная масса конечной смеси равна 1,2*4 = 4,8 г/моль. Мольное отношение газов в смеси - оставшегося муравьиного альдегида к оставшемуся водороду соответственно) равно (4,8 - 2):(30 - 4,8) = 1:9. И тогда (0,3 - х)/(0,7 - х) = 1/9, откуда х = 0,25 моль. Это практический выход.
Выход продукта реакции равен 0,25:0,3 = 0,833, или 83,3%