Концентрированные серная и азотная кислоты являются сильными окислителями. В азотной кислоте окислителем служит азот в степени окисления +5, в серной кислоте – сера в степени окисления +6: Cu + 2H2SO4(конц.) ⟶ CuSO4 + SO2↑ + 2H2O S+6 + 2ē ⟶ S+4 1 окислитель (восстановление) Cu0 - 2ē ⟶ Cu+2 1 восстановитель (окисление) Cu + 4HNO3(конц.) ⟶ Cu(NO3)2 + 2NO2↑ + 2H2O N+5 + 1ē ⟶ N+4 2 окислитель (восстановление) Cu0 - 2ē ⟶ Cu+2 1 восстановитель (окисление) Различие в свойствах серной и азотной кислот. Разбавленная серная кислота реагирует с металлами с выделением водорода, то есть окислителем служит водород в степени окисления +1: Mg + H2SO4 ⟶ MgSO4 + H2↑ 2H+ + 2ē ⟶ H20 1 окислитель (восстановление) Mg0 - 2ē ⟶ Cu+2 1 восстановитель
Электроотрицательность
Объяснение:
Это атома, связанного с другим атомом, притягивать к себе связующее электронное облако, вызывая тем самым поляризацию ковалентной связи.
Электроотрицаиельность—атома условная величина, характеризующая атома в молекуле приобретать отрицательный заряд (притягивать электроны). Зная электроотрицательность, можно определить полярность ковалентной связи, вычислить эффективные заряды атомов и др...
————
фундаментальное химическое свойство атома, количественная характеристика атома в молекуле притягивать к себе общие электронные пары.
Первая и широко известная шкала относительных атомных электроотрицательностей Полинга охватывает значения от 0,7 для атомов цезия до 4,0 для атомов фтора. Фтор — наиболее электроотрицательный элемент, за ним следует кислород (3,5) и далее азот и хлор (3,0). Активные щелочные и щёлочноземельные металлы имеют наименьшие значения электроотрицательности, лежащие в интервале 0,7—1,2, а галогены — наибольшие значения, находящиеся в интервале 4,0—2,5. Электроотрицательность типичных неметаллов находится в середине общего интервала значений и, как правило, близка к 2 или немного больше 2. Электроотрицательность водорода принята равной 2,1. Для большинства переходных металлов значения электроотрицательности лежат в интервале 1,5—2,0. Близки к 2,0 значения электроотрицательностей тяжёлых элементов главных подгрупп. Существует также несколько других шкал электроотрицательности, в основу которых положены разные свойства веществ. Но относительное расположение элементов в них примерно одинаково.
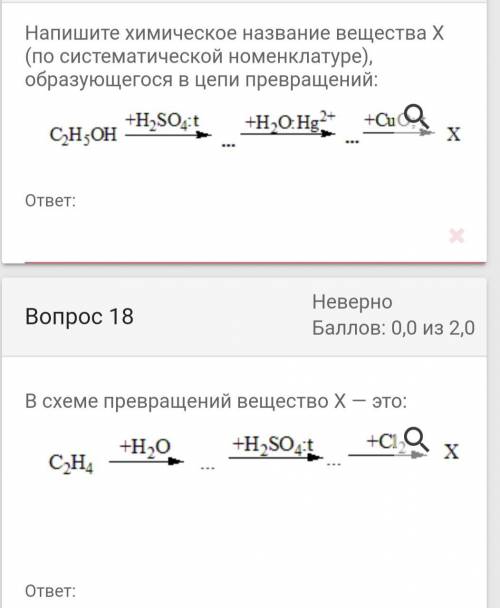
1) c2h5oh + h2so4 -> -H2O + c2h4
c2h4 + h2o -> c2h5oh
c2h5oh + cuo2 -> ch3cooh (этановая кислота)
2) c2h4 + h2o -> c2h5oh
c2h5oh + h2so4 -> c2h4
c2h4 + cl2 -> c2h4cl2 (1,2-дихлорэтан)
Объяснение: