Дано:
ω(O₂) = 30%
ω(SO₂) = 70 %
---------------------------
Найти:
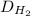 (смеси) - ?
(смеси) - ?
1) Для вычисления плотности газовой смеси по водороду нам понадобится значение ее средней молярной массы. Ее найдем вот по формуле:
M(смеси) = (ω(O₂)×М(O₂)) + (ω(SO₂)×М(SO₂)) = (30% × 32 гр/моль) + (70% × 64 гр/моль) = (0,3 × 32 гр/моль) + (0,7 × 64 гр/моль) = 9,6 гр/моль + 44,8 гр/моль = 54,4 гр/моль
2) Для начала мы найдем молекулярные массы кислорода и оксида серы(IV) и водорода, а потом мы находим молекулярную смеси газов под пунктом 1) :
M(O₂) = 16×2 = 32 гр/моль
M(SO₂) = 32+16×2 = 32+32 = 64 гр/моль
M(H₂) = 1×2 = 2 гр/моль
3) Потом мы находим плотность по водороду газовой смеси по такой формуле:
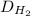 (смеси) = M(смеси)/M(H₂) = 54,4 гр/моль / 2 гр/моль = 27,2
(смеси) = M(смеси)/M(H₂) = 54,4 гр/моль / 2 гр/моль = 27,2
ответ: 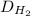 (смеси) = 27,2
(смеси) = 27,2
Дано:
m теор.(C₆H₁₂O₆) = 400 гр
m практ.(C₂H₅OH) = 203 гр
Найти:
η(C₂H₅OH) - ?
1) Запишем уравнение реакций:
C₆H₁₂O₆ (дрожжи) → 2C₂H₅OH + 2CO₂
2) Для начала мы найдем количество вещества глюкозы, а потом этилового спирта:
M(C₆H₁₂O₆) = 12×6+1×12+16×6 = 72+12+96 = 180 гр/моль
n(C₆H₁₂O₆) = m(C₆H₁₂O₆)/M(C₆H₁₂O₆) = 400 гр / 180 гр/моль ≈ 2,22 моль ⇒ n(C₂H₅OH) = 2n(C₆H₁₂O₆) = 2 × 2,22 моль = 4,44 моль
3) Далее мы находим массу этилового спирта теоретического:
M(C₂H₅OH) = 12×2+1×5+16+1 = 24+5+17 = 46 гр/моль
m теор.(C₂H₅OH) = n(C₂H₅OH) × M(C₂H₅OH) = 4,44 моль × 46 гр/моль = 204,24 гр
4) Теперь находим процент выхода продукта:
η(C₂H₅OH) = m практ.(C₂H₅OH) / m теор.(C₂H₅OH) × 100% = 203 гр/204,24 гр × 100% ≈ 0,9939 × 100% ≈ 99,39%
ответ: η(C₂H₅OH) = 99,39%