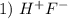 ⇒
⇒ 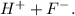
еще тогда, когда не была точной наукой, в древние времена и эпоху средневековья, ученые и ремесленники иногда случайно открывали способы получения и очистки многих веществ, находивших применение в хозяйственной деятельности: металлов, кислот, щелочей, красителей и т.д. точной наукой начала становится только в 19 веке, когда был открыт закон кратных отношений и разрабатывалось атомно-молекулярное учение. современные техники хроматографии позволяют быстро отделить вещество от примесей и проверить его индивидуальность. кроме того, для очистки веществ широко применяются классические, но сильно усовершенствованные приемы перегонки, экстракции и кристаллизации. методы исследования веществ, разработанные и -, приносят пользу не только в , но и в смежных науках: , биологии, геологии. без них уже не могут обойтись ни промышленность, ни сельское хозяйство, ни медицина, ни криминалистика. - приборы занимают почетное место на космических аппаратах, с которых исследуют другие планеты и околоземное пространство
m(Mg+MgO) = 6 g
V(H2)- 2.4 L
W(MgO) - ?
1) Mg+2HCL-->MgCL2+H2
2) MgO+2HCL-->MgCL2+H2O
Обратим внимание , что в реакции (1) выделился водород , во (2) нет
Находим массу магния по объему выделившего водорода
Mg+2HCL-->MgCL2+H2
M(Mg) = 24 g/mol
Vm = 22.4 L/mol
X / 24 = 2.4 / 22.4
X = 2.58 g - столько находится магния в смеси
зная . массу смеси и массу магния , определяем массу оксида магния
m(MgO) = m(Mg+MgO) - m(Mg) = 6 - 2.58 = 3.42 g
Определяем массовую долю MgO
W(MgO) = m(MgO) / m(Mg+MgO) / 100% = 3.42 / 6 * 100% = 57%
ответ 57%
Объяснение: