Химия – основоположная экспериментальная наука, используемая в различных сферах жизни. Медицина, производство, сельское хозяйство, промышленность, нефтедобыча, металлургия, косметология, машиностроение – далеко не все отрасли, основанные на применении химических реакций. На стыке химии и других наук возникло множество популярных, хорошо оплачиваемых профессий. Биотехнолог, биоинженер, нанотехнолог, эколог, биохимик – в числе топовых должностей, связанных с работой в международных компаниях. Пользуются спросом постоянно актуальные профессии – врач, фармацевт, провизор, ветеринар.
В процессе школьного обучения химия представляется сложной дисциплиной. Однако если досконально изучить таблицу Менделеева, валентность, тонкости химических переходов и взаимодействий, данная наука выглядит логически обоснованной. Школа не дать всю полноту необходимых знаний – нужно обратиться за профессиональной педагогической . Репетитор по химии наглядно усвоить закономерности химических реакций и процессов.
Занятия с педагогом раскрыть предмет с нетипичной точки зрения. Ученик получает:
• полезный практический опыт проведения экспериментов;
• разнообразные увлекательные задания;
• прикладное применение теории;
• обеспечение качественными учебными материалами
Точные науки – фундамент успешной профессии!
Математика, физика, химия непременно пригодятся в современной жизни. Связав с ними будущую специальность, школьник получит стопроцентную гарантию востребованности на рынке труда.
Перечисленные предметы невозможно заучить. Главное – научиться критически мыслить и анализировать. С частного репетитора ребенок сможет отточить логику, широту суждения, развить аналитико-оценочные . Точные науки дисциплинируют ум, шлифуют его глубину и скорость быстро решать практические задачи.
Занятия с педагогом вырабатывают навыки самостоятельности, находчивости, многозадачности. Комбинация данных дисциплин развивает эрудированность и готовит будущего специалиста к любым профессиональным вызовам.
Объяснение:
Объяснение:
Высший оксид вида
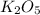
характерен для элементов
V группы а-подгруппы (N, P, As, Sb, Bi)
в таблице Менделеева
Для этих же элементов характерен гидрид вида:
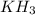
Известно, что в соединении с гидрогеном (водород, Н) массовая доля гидрогена составляет 8.8%.
Напишем уравнение
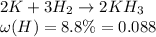
Молекулярная масса КН3 равна:
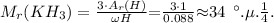
Следовательно, атомная масса элемента К равна:

И действительно в V группе а-подгруппе есть элемент с атомной массой 31 а.е.м.
И этот элемент - фосфор (Р)
Это 15 элемент в Таблице. Его электронная формула имеет вид:
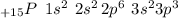
Гидрат оксида фосфора, который соответствует его высшему оксиду (гидроксид фосфора) - это фосфорная кислота, чаще всего имеется в виду ортофосфорная кислота
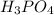
однако может встречаться и метафосфорная кислота
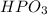
Фосфорная кислота реагирует с
с основными оксидами:
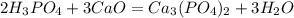
с основаниями:
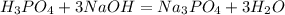
Характерная реакция на фосфат-ионы - взаимодействие с нитратом серебраAgNO3. При этом образуется ярко-желтый осадок фосфата серебра:

2K₂FeO₄ + 16HCl → 3Cl₂ + 4KCl + 2FeCl₃ + 8H₂O
Fe⁺⁶ + 3e → Fe³⁺ - окислитель
2Cl⁻ - 2e → Cl₂⁰ - восстановитель
Не совсем понятен вопрос. При окислителе коэффициент 2, при восстановителе 3.