HCOOH + KOH = HCOOK + H2O. Образовался формиат калия.
m(KOH)=28 г - масса гидроксида калия
m(HCOOK)=18,4 г - это масса муравьиной кислоты
M(HCOOK)=1+12+32+39=84 г/моль
M(KOH)=39+16+1=56 г/моль
n(KOH)=m/M=28г / 56 г/моль=0,5 моль
n(HCOOK)=18,4г / 84 г/моль=0,22 моль
Найдём массовую долю (составим пропорцию):
0,5 моль/0,22 моль = 100%/х --> х=44%
Дальше по этой формуле вывести m(р-в.)и подставить числа
W= m(р.в) / m(р-ра) * 100%
ответ: 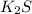
Объяснение к ответу: Начнём с условия. В условии сказано, что в формуле на первом месте нужно записать химический знак элемента. Химический элемент из самого условия это Калий, его знак это K. Ставим теперь этот химический знак, далее по условию "на втором — химический знак серы." Это значит, что после К мы пишем химический знак серы S. Мы знаем, что индекс - это число, показывающее количество атомов данного химического элемента в молекуле вещества. Индекс у нас равен 2, так как в соединении калия с серой: сера имеет валентность равную II, а калий I. Значит у Калия индекс будет 2, а у Серы 1.
На заметку: Соединения с серой называются сульфидами и сера в таких соединениях имеет степень окисления -2 или валентность равную двум.
HCOOH + KOH = HCOOK + H2O
n(HCOOH) = m(HCOOH)/M(HCOOH) = 18.4/46 = 0.4моль
n(KOH) = m(KOH)/M(KOH) = 28/56 = 0.5моль
соотношение по уравнению 1:1, значит, HCOOH дана в недостатке, а KOH-в избытке. Задача решается по недостатку:
n(HCOOH) = n(HCOOK) = 0.4моль
m(HCOOK) = n(HCOOK)*M(HCOOK) = 0.4*84 = 33.6г