1) Электролиз:
2NaBr = 2Na + Br2.
2) Это гальванический элемент Даниэля:
Две разделенные перегородкой емкости. В одной цинковый электрод, погруженный в раствор сульфата цинка, в другой - медный электрод, погруженный в раствор сульфата меди. При замыкании цепи образуется эл. ток вызванный эдс, равной примерно разности стандартных электродных потенциалов меди и цинка. (При условии примерно равной концентрации растворов сульфатов меди и цинка).
Е = Е(Cu) - E(Zn) = 0,337 - (-0,763) = 1,1 В.
Формула окислительно-восстановительной реакции:
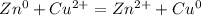
3) Уравнения гидролиза CH3COOK:
В молекулярной форме:
CH3COOK + H2O = CH3COOH + KOH.
В полной йонной форме:
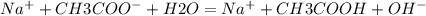
В сокращенной ионной форме:

Слабая кислота и сильное основание дают щелочную реакцию с pH>7.
4) По определению молярности раствора:
0,2 = m/(M*V), где m - искомая масса соли, M = M(NaNO3) = 85 г/моль,
V = 400 мл = 0,4 л.
m = 0,2*0,4*85 = 6,8 г
ответ: 6,8 г.
5) 4H2O2 + 4KMnO4 = 4MnO2 + 4KOH + 5O2 + 2H20
Перманганат(MnO4^(-1)) выступает в роли окислителя, а конкретно - марганец. Он принимает 3 электрона и степень окисления становится (+4)
Mn(+7) + 3e = Mn(+4)
Еще в роли окислителя выступают два иона ОН в перекиси водорода:
2ОН(0) + 2е = 2ОН(-1)
Кислород восстановитель
2О(-2) - 4е = О2(0)
Теперь выставляем коэффициенты по диагонали, делая электронный баланс. Перед свободным кислородом ставим коэффициент (3+2) = 5, а перед перекисью и марганцовкой ставим по 4. Остальные коэффициенты получаются автоматически.
ZnO+2H+ + SO4 2- >H2O + Zn2+ + SO4 2-
ZnO+2H+ --->H2O + Zn2+
Ca(OH)2+2HNO3-->2H2O+Ca(NO3)2
Ca2+ + 2OH- +2H+ + 2NO3- >2H2O + Ca2+ + 2NO3-
2OH- +2H+-->2H2O
3KOH+H3PO4-->3H2O + K3PO4
3K+ + 3OH- + 3H+ + PO4 3- > 3H2O +3K+ + PO4 3-
3OH- + 3H+ --->3H2O
Fe(OH)3+3HCl -->FeCl3+3H2O
Fe3+ + 3OH- + 3H+ +3Cl- >Fe3+ + 3Cl- + 3H2O
3OH- + 3H+ --->3H2O
2NaOH+H2SO4-->2H2O + Na2SO4
2Na+ +2OH- + 2H+ +SO4 2- --->2H2O + 2Na+ + SO4 2-
2OH- + 2H+ -->2H2O
CaCl2+H2SO4-->CaSO4 + 2HCl
Ca2+ 2Cl- + 2H+ +SO4 2- >Ca2+ +SO4 2- + 2H+ +2Cl-