1.У атомов водорода и фосфора почти одинаковые значения ЭО. Какой тип химической связи в молекуле фосфина PH3? 2. Определите тип химической связи и запишите схему её образования для веществ с формулами:
а) S2, K2O и H2S; б) N2, Li3N и Cl3N.
3. В какой из молекул - хлороводорода HCl или фтороводорода HF - ковалентная химическая связь более популярна?
4. В следующих предложениях впишите пропущенные слова и выражения: «Ковалентная химическая связь образуется за счёт ... . По числу общих электронных пар она бывает ... . По ЭО ковалентную связь делят на ... и ...».
5. Определите валентности элементов в соединениях с формулами:
PbS, PbO2, FeS2, Fe2s3, SF6.
6. Запишите формулы хлоридов - соединений элементов с одновалентным хлором: железа(III), меди(I), меди(II), марганца(IV), фосфора(V).
что есть
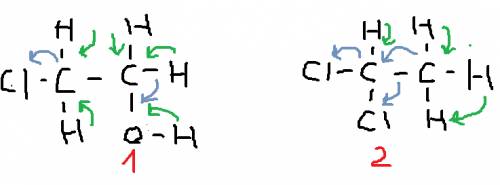
1)ковалентная неполярная (в качестве исключения)
2)S2, K2O и H2S- ковалентная неполярная, ионная и ковалентная полярная
N2, Li3N и Cl3N- ковалентная неполярная, ионная и ковалентная неполярная(искл как фосфин)
3)HF
4)общих электронных пар
простая,двойная,тройная
полярную и неполярную
5)PbS-2,2
PbO2-4,2
FeS2-2,2
Fe2s3- 3,2
SF6-6,1
6) железа(III)- FeCl3
меди(I)- CuCl
меди(II)-CuCl2
марганца(IV)- MnCl4
фосфора(V)- PCl5
Объяснение: