Объяснение:
Определи объём (н. у.) газа, который выделится при действии 200 г 4,9%-ного раствора серной кислоты на карбонат бария.
0,1 моль 0,1 моль
BaCO3 + H2SO4 = BaSO4↓ + Н2О + СО2↑
Масса серной кислоты в растворе: 200 г × 0,049 = 9,8 г. Эта масса серной кислоты соответствует 0,1 моль Н2SO4.
Тогда по уравнению реакции количество углекислого газа составит также 0,1 моль. Объем СО2 при н.у. составит 2,24 дм3
Точность промежуточных вычислений — до тысячных. ответ округли до сотых. Например: 4,36.
ответ: объём газа равен 2,24 дм3
дм³.
Найди массу раствора хлорида магния с массовой долей соли 0,02, которую надо добавить к нитрату серебра для получения осадка химическим количеством 0,4 моль.
0,4 моль
MgCl2 + 2AgNO3 = 2AgCl + Mg(NO3)2
По уравнению реакции количество вещества хлорида магния составит 0,2 моль. Молярная масса MgCl2 равна 95 г/моль. Отсюда масса m(MgCl2) = 95 г/моль × 0,2 = 19 г
Масса раствора хлорида магния 19 г : 0,02 = 950 г
К сведению составителей задач. Нитрат серебра очень дорогой препарат и приучать студентов и может будущих сотрудников к экономии необходимо уже на на уровне решения задач.
Точность промежуточных вычислений — до сотых. ответ округли до целых. Например: 367.
ответ: масса раствора равна 950 г
г.
Какая масса раствора азотной кислоты с массовой долей HNO3, равной 0,15, потребуется для реакции с 14 г оксида алюминия?
52,9г 14 г
6НNO3 + Al2O3 = 2Al(NO3)3 + 3H2O
0,84 моль 0,14 моль
М(Al2O3) = 102 г/моль
Найдем количество оксида алюминия: 14 г : 102 г/моль = 0,14 моль.
Тогда количество азотной кислоты составит 0,14 моль × 6 = 0,84 моль, а масса азотной кислоты 63 г/моль × 0,84 моль = 52,9 г
Вычислим массу раствора азотной кислоты: 52,9 г : 0,15 = 353 г
Точность промежуточных вычислений — до сотых. ответ округли до целых. Например: 367.
ответ: масса раствора равна 353 г
г.
Какая масса 10%-ного раствора нитрата магния прореагирует с 250 г 2%-ного раствора гидроксида калия?
0,045 моль 0,09 моль
Mg(NO3)2 + 2KOH = Mg(OH)2 ↓ + 2KNO3
Вычислим массу гидроксида калия, содержащегося в 2% растворе
КОН. m(KOH) = 250 г × 0,02 = 5 г
Эта масса гидроксида калия соответствует 5 г : 56 г/моль = 0,09 моль. Тогда в реакцию с 0,09 моль КОН вступит 0,045 моль
нитрата магния. Рассчитаем массу нитрата магния и массу его 10% раствора. Молярная масса нитрата магния равна 148 г/моль.
m Mg(NO3)2 = 148 г/моль х 0,045 моль = 6,66 г
А масса раствора = 6,66 г : 0,1 = 67 г
Точность промежуточных вычислений — до тысячных. ответ округли до десятых. Например: 367.
ответ: масса раствора нитрата магния равна 67 г
г.
Відповідь:
3. m(раствора) =298.4 г
4. m(раствора)=98,67 g
Пояснення:
Задача 3. Дано: w(HNO₃)=0.15 . m(Cr₂O₃)=18 gI. Запишем реакцию:
6 HNO₃ + Cr₂O₃ → 3 H₂O + 2 Cr(NO₃)₃
С реакции видно, что соотношение количества между реагентами, как 6:1. Тоесть, 6n(HNO₃)=n(Cr₂O₃)
II. Запишем формулы // Проведем вычисления:
n(E)=m(E)/Mr(E)
m(E)=n(E)*Mr(E)
w(E)=m(E)/m(раствора)
Запишем соотношение за количеством вещества:
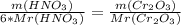
m(HNO₃)=m(Cr₂O₃)*6Mr(HNO₃)/Mr(Cr₂O₃)
m(HNO₃)=18*6*63/152=44.76 g
Подставляем эту массу формулу массовой доли:
0.15=44.76/m(раствора)
m(раствора) = 44.76/0.15=298.4 г
Задача 4. w(Mg(NO₃)₂)=15% w(NaOH)=8% m(раствора NaOH)=100gI. Запишем реакцию:
Mg(NO₃)₂ + 2 NaOH → 2 NaNO₃ + Mg(OH)₂ ↓
С реакции видно, что соотношение количества между реагентами, как 1:2. Тоесть, нужно 1х моль Mg(NO₃)₂ и 2x моль NaOH.
II.Запишем формулы // Проведем вычисления:
n(E)=m(E)/Mr(E)
m(E)=n(E)*Mr(E)
w(E)=m(E)/m(раствора) · 100%
m(E)=w(E)*m(розчину) / 100%
m(NaOH)=100*8/100=8 g
n(NaOH)=8/40=0.2 моль
n(Mg(NO₃)₂)=0.2/2=0.1 моль
m(Mg(NO₃)₂)=0.1*148=14.8 g
15 = 14.8 · 100% / m(раствора)
m(раствора)=14.8 · 100% / 15=98,67 g
*Поставьте лучшее
онечно, любой знает, что многие средства для чистки дома содержат химию, которая может принести ему вред или даже убить его, если он выпьет это средство. Но отравление может наступить и другим путем. Вы можете вдыхать испарения химикатов и они будут попадать в вашу кровь через легкие. Химикаты могут попадать на вашу кожу и они будут впитываться через нее. Кожа может впитать намного больше чем вы можете себе представить. В сущности, токсичные химикаты могут попадать в организм при приеме их внутрь, при вдохе, при прикосновении, и даже при прикосновении к предмету на который было нанесено токсичное вещество дни и месяцы назад.
Семьдесят тысяч новых химикатов было открыто во времена Второй Мировой Войны в результате исследований в химической военной промышленности! 250 миллиардов фунтов (113.25 миллиардов килограмм) синтетических химикатов производится каждый год в США (согласно California Public Interest Research Group) ! Сейчас тысячи этих химикатов появились безобидно на полках ваших магазинов - для чистки вашей одежды, вашего пола, ваших волос, ваших зубов и ваших печей. И только потому что эта продукция стоит на полках магазинов, вы думаете, что она безопасна для вас и вашей семьи! Мы первое поколение которое выросло с таким экстремально высоким уровнем химикатов в наших домах.