
Кисень O2, вуглекислий газ СO2, озон O3 — важчі за повітря.
Щоб довести це, скористаємося наслідком із закону Авогадро. Порівняємо маси газів, що відповідають об’єму 22,4 л. Кількість речовини газів, що міститься у цьому об’ємі, дорівнює 1 моль, а маса дорівнюватиме молярній масі.
М(повітря) = 29 г/моль, М(O2) = 32 г/моль, М(СO2) = 44 г/моль, М(O3) = 48 г/моль.
Отже, маса 22,4 л кисню, взятого за нормальних умов, становитиме 32 г, а маса такого самого об’єму повітря — 29 г.
Відносна густина показує, у скільки разів один газ важчий за інший. Розрахуємо відносну густину кисню, вуглекислого газу, озону за повітрям.
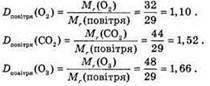
1. В основу своей классификации химических элементов Д. И. Менделеев положил относительную атомную массу.
2. Менделеев формулировал периодический закон так: "Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов".
3. Закон был назван периодическим, поскольку свойства элементов меняются периодично, с заданной периодичностью.
4. 1) Химический знак натрия - Na;
Порядковый номер элемента - 11;
Номер периода - 3;
Номер группы - 1;
Номер подгруппы - главная (А) подгруппа;
3)Формула оксида - Na2O;
4) Характер оксида - основный;
5) Формула гидроксида - NaOH;
6) Характер гидроксида - основание;
7) 1. Основные оксиды взаимодействуют с водой с образованием оснований. Непосредственно в реакцию соединения с водой вступают только оксиды щелочных и щелочноземельных металлов:
Na2O + H2O → 2NaOH,
CaO + H2O → Ca(OH)2.
2. Взаимодействие с кислотами с образованием соли и воды:
CaO + H2SO4 → CaSO4 + H2O.
3. Взаимодействие с кислотными оксидами с образованием соли:
СaO + SiO2=(под действием температуры) CaSiO3
4. Взаимодействие с амфотерными оксидами:
СaO + Al2O3 =(под действием температуры)Сa (AlO2)2.
Дано: білі порошки у пробірках: KNO3, Na2CО3, і СаСО3.
Додаємо в пробірки воду.
В пробірці з СаСО3 осад не розчиняється, тому що СаСО3 — нерозчинна речовина.
До пробірок з розчинами Na2CO3 і KNO3 додаємо сульфатну кислоту:
гаємо "вскипання".
2Na+ + CO32- + 2H+ + SO42- = 2Na+ + SO42- + CO2↑ + H2O
2H+ + CO32- = CO2↑ + H2O
2KNO3 + H2SO4 = K2SO4 + 2HNO3 - розчин не змінюється.
2K+ + 2NO3- + 2H+ + SO42- = 2K+ +SO42- + 2H+ +NO3-