1. CO2 - сложное вещество, с ковалентной полярной связью, состоит из двух элементов - углерод со степенью окисления +4 и кислорода со степенью окисления -2, валентность углерода (IV), кислорода (II);
2. Название элемента, символ, порядковый номер, относительную атомную массу, в некоторых таблицах предоставлен внешний энергетический слой и электронная конфигурация;
3. H2 - водород, Br2 - бром, U - уран;
4. Cl2O7 - оксид хлора (VII), C6H5-C6H5 - дифенил, B2H6 - диборан;
5. Любое определенное химически чистое соединение, независимо от его получения, состоит из одних и тех же химических элементов, причём отношения их масс постоянны, а относительные числа их атомов выражаются целыми числами;
Масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ. При химических реакциях атомы не исчезают и не появляются. Продукты реакции образуются из атомов, содержащихся в исходных веществах. Поэтому масса и остаётся неизменной;
Согласно закону Авогадро, одно и то же количество молекул любого газа занимает при одинаковых условиях один и тот же объём. С другой стороны, 1 моль любого вещества содержит, по определению, одинаковое количество частиц, например, молекул. Отсюда следует, что при определённых температуре и давлении 1 моль любого вещества в газообразном состоянии занимает один и тот же объём.
Объяснение:
Думаю, вывод Вы сами напишите)
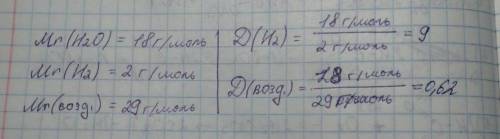
1)HCl
HCl+AgNO3===>AgCl(стрелка вниз) + HNO3
H(+) + Cl(-) + Ag(+) + NO3(-)===>AgCl(стрелка вниз) + H(+) + NO3(-)
Cl(-) + Ag(+)===>AgCl(стрелка вниз)
При взаимодействии соляной кислоты с нитратом серебра выпадает белый осадок AgCl.
2)H2SO4
H2SO4+BaCl2>BaSO4(стрелка вниз) + 2HCl
2H(+) + SO4(2-) + Ba(2+) + 2Cl(-)===>BaSO4(стрелка вниз) + 2H(+) + 2Cl(-)
SO4(2-) + Ba(2+)===>BaSO4(стрелка вниз)
При взаимодействии хлорида бария с серной кислотой выпадает белый осадок BaSO4.
3)HNO3
4HNO3+Cu===>Cu(NO3)2+ 2NO2(стрелка вверх) + 2H2O
4H(+) + 4NO3(-) + Cu===>Cu(2+) + 2NO3(-) + 2NO2(стрелка вверх) + 2H2O
4H(+) + 2NO3(-) + Cu===>Cu(2+) + 2NO2(стрелка вверх) + 2H2O
При взаимодействии азотной кислоты с медью образуется раствор голубого цвета и бурый газ NO2.
4 P + 5O2 —> 2P2O5 - соединения
2HgO —> 2Hg + O2 - разложения
Zn + 2HCl —> ZnCl2 + H2 - замещения
HCl + KOH —> KCl + H2O - обмена
CaO + H2O —> Ca(OH)2 - соединения
Cu2CH2O5—> 2CuO + H2O +CO2 - разложения
Cu(OH)2—> CuO + H2O - разложения
2CO + O2—> 2CO2 - соединения
BaCl2 + H2SO4—> BaSO4 + 2HCl - обмена
FeO + 2HCl —> FeCl2 + H2O - обмена