Задача 14: 3.76 грамм
Задача 16: 0.8 к 1.8 или 1 к 2.25
Объяснение:
Задание 14:
Mr[Cu(NO3)2] = 188 г/моль
Число атомов: 1Cu + 2N + 6O = 9 атомов всего
N (A) = 9 × 6.02 × 10^23 = 54.18 × 10^23 атомов
N(A) = 1.0835 × 10^23 атомов
m[Cu(NO3)2] = ?
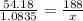
x= 3.76 грамм
m[Cu(NO3)2] = 3.76 грамм
ответ: 3.76 грамм
Задание 16:
Ca3(PO4)2
Mr(соли) = 310 грамм/моль
n(P) = 2 моль атомов фосфора в составе 1 моли соли
m(соли) = 124 грамм
n(соли) = m/Mr = 124/310 = 0.4 моли
n(P) = 2 × 0.4 = 0.8 моль Фосфора в составе соли массой 124 грамма
Al(NO3)3
Mr(соли) = 213 грамм/моль
n(N) = 3 моль атомов азота в составе 1 моли соли
m(соли) = 127.8 грамм
n(соли) = m/Mr = 127.8 / 213 = 0.6 моли
n(N) = 3 × 0.6 = 1.8 моль азота в составе соли массой 127.8 грамм
Соотношение:
n(P) = 0.8
n(N) = 1.8
0.8 к 1.8
или
1 к 2.25
1.
СuO + H₂SO₄ = CuSO₄ + H₂O
CuSO₄ + 2KOH = Cu(OH)₂ + K₂SO₄
Cu(OH)₂ = CuO + H₂O
2.
Дано:
m(H₂SO₄) = 9,8 г
m(BaCl₂) = 4,6 г
Найти:
m(BaSO₄)-?
Решение.
M(H₂SO₄) = 98 г/моль
n(H₂SO₄) = m/M = 9,8 г/98 г/моль = 0,1 моль
M(BaCl₂) = 208 г/моль
n(BaCl₂) = m/M = 4,6 г/208 г/моль = 0,022 моль
H₂SO₄ + BaCl₂ = BaSO₄ + 2HCl
Из УХР видно, что n(H₂SO₄):n(BaCl₂) = 1:1, а исходя из расчетов по условию задачи n(H₂SO₄):n(BaCl₂) = 0,1:0,022 = 4,5:1, следовательно, серная к-та взята в избытке. Расчеты производим по хлориду бария, исходя из УХР n(BaSO₄)=n(BaCl₂); n(BaSO₄) = 0,022 моль
М(BaSO₄) = 233 г/моль
m(BaSO₄) = n*M = 0,022 моль*233 г/моль = 5,1 г
ответ: 5,1 г
3.
1) Отделяем железные опилки с магнита
2) Останется соль с древесными опилками. Заливаем водой в колбе, перемешиваем до полного растворения соли.
3) фильтруем смесь, древесные опилки останутся на фильтре, останется раствор соли
4) Выливаем раствор соли в фарфоровую чашку, которую ставим на штатив, под чашку ставим спиртовку, соблюдая технику безопасности, поджигаем спиртовку, регулируем высоту с зажима и выпариваем воду из раствора поваренной соли. После выпаривания воды в чашке останется очищенная поваренная соль.