Дано:
CO₂
V = 1 мл = 1×10⁻⁶ м³
t = 27°C
p = 20 кПа = 20×10³ Па
Найти:
n(CO₂) - ?
1) Для нахождения молекул у оксида углерода (IV) используется формула Менделеева-Клайперона именно по такой формуле мы будем пользоваться:
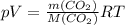 - Формула Менделеева-Клайперона
- Формула Менделеева-Клайперона
2) Из формулы Менделеева-Клайперона мы найдем массу оксида углерода (IV), но сначала мы найдем температуру в кельвинах, а потом его молекулярную массу:
T = t + 273 = 27 + 273 = 300 К
M(CO₂) = 12 + 16×2 = 12 + 32 = 44 гр/моль
m(CO₂) = (pV×M(CO₂))/RT = (20×10³ Па × 1×10⁻⁶ м³ × 44 гр/моль)/(8,31 Дж/(моль×К) × 300 К) = (2×10⁻² Дж × 44 гр/моль)/2493 Дж/моль ≈ 8,02×10⁻⁶ моль × 44 гр/моль ≈ 352,88×10⁻⁶ гр ≈ 3,5288×10⁻⁴ гр
3) Теперь находим количества вещества у оксида углерода (IV):
n(CO₂) = m(CO₂)/M(CO₂) = 3,5288×10⁻⁴ гр / 44 гр/моль = 8,02×10⁻⁶ моль
ответ: n(CO₂) = 8,02×10⁻⁶ моль
Решено от : 
Это означает что в 40 г 20% р-ра серной кислоты содержится 8 г серной кислоты.
Примем массу 30% раствора серной кислоты за х г, а массу 5% р-ра серной кислоты за у г, тогда при смешивании этих двух р-ров, их масса должна составить 40 г, т.е. х+у=40, а 0,3х+0,05у=8. Получилась система двух уравнений, решив ее, найдем х, х - это масса 30% р-ра и она равна 24 г, а масса 5% р-ра = 40 г - 24 г = 16 г
Вывод: Для приготовления 40 г 20% р-ра серной к-ты необходимо взять 24 г 30% р-ра серной к-ты и 16 г 5% р-ра серной к-ты.
ответ: 24 г и 16 г.