1) Ток проводят: Na₂CO₃, Ca(OH)₂, HF, H₂SO₄
Сильные электролиты: Na₂CO₃, H₂SO₄
Слабые электролиты: Ca(OH)₂, HF
Na₂CO₃ → 2Na+ + CO₃(2-)
Ca(OH)₂ ⇄ Ca(2+) + 2OH-
HF ⇄ H+ + F-
H₂SO₄ → 2H+ + SO₄(2-)
2) a) KNO₃ + HCl ⇸
б) BaCl₂ + H₂SO₄ → BaSO₄ + 2HCl
Ba(2+) + 2Cl- + 2H+ + SO₄(2-) → BaSO₄ + 2H+ + Cl-
Ba(2+) + SO₄(2-) → BaSO₄
в) Ca + 2HCl → CaCl₂ + H₂↑
Это реакция не ионного обмена, поэтому ионных уравнений здесь нет
г) ZnSO₄ + 2KOH → Zn(OH)₂ + K₂SO₄
Zn(2+) + SO₄(2-) + 2K+ + OH- → Zn(OH)₂ + 2K+ + SO₄(2-)
Zn + 2OH- → Zn(OH)₂
д) CuO + 2HNO₃ → Cu(NO₃)₂ + H₂O
CuO + 2H+ + NO₃- → Cu(2+) + NO₃- + H₂O
CuO + 2H+ → Cu(2+) + H₂O
6) щелочи: NaOH, KOH, LiOH,Ca(OH)2
нерастворимые: Ti(OH)3, Mg(OH)2
9) KOH + HNO3= H2O + KNO3
n=m÷M
n(HNO3) = 18,9÷63= 0,3 моль
по уравнению следует, что: n(HNO3)= n(KNO3)=0,3 моль
m=n×M
m(KNO3) = 0,3 × 101= 30,3 г
ответ:30,3г
10) из дано этот элемент щелочноземельный металл, все ЩЗМ реагируют с азотом одинаково(азот восстанавливается до -3), примем щзм за Х:
3X+N2=X3N2
n= V÷Vm
(для газов при н.у. Vm=22,4 л/моль)
n(N2) = 1,12:22,4= 0,05 моль
по уравнению реакции: 3×n(N2)= n(X)
n(X)= 0,05×3= 0,15 моль
M=m÷n
M(X)=3,6÷0,15=24г/моль => Х - это Мg
схема электронного строения на фото
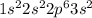
Н2+О2=2NO-90,4кДж(сполучення, окисно-відновна, екзотермічна, оборотна)
СаСО3=СаО+СО2-157кДж(розкладу, ендотермічна)
2NO+O2=2NO2+116кДж(сполучення, окисно-відновна, екзотермічна, оборотна)
2СО+О2=2СО2; ∆Н=-566кДж(сполучення, окисно-відновна, екзотермічна)
2НBr=H2+Br2;∆H=+72кДж,(розкладу, окисно-відновна, екзотермічна)