Відповідь:
1. Фоточка - 1.png
2. 2Al + 3S → Al₂S₃
Al₂S₃ + 6H₂O → 3H₂S↑ + 2Al(OH)₃
Al(OH)₃ + KOH → K[Al(OH)₄]
K[Al(OH)₄] → KAlO₂↓ + 2H₂O
KAlO₂ + 4HCl → KCl + AlCl₃ + 2H₂O
3. Ag + 2HNO₃ →AgNO₃ + NO₂↑ + H₂O
n(E)=m(E)/Mr(E)
n(Ag)=21.6/108=0.2 моль
m(HNO₃)=600*0.68=408g
n(HNO₃)=408/63=6.5 моль
Значит, азотная кислота в избытке, считаем по серебру:
n(NO₂)= 0.2 моль
2NO₂+ 2NaOH → NaNO₂ + NaNO₃ + H₂O
m(NaOH)=300*0.1=30г
n(NaOH)=30/40=0.75 моль
Значит, NaOH в избытке.
n(NaNO₂)=0.1 моль
m(NaNO₂)=0.1*69=6.9 г
n(NaNO₃)=0.1 моль
m(NaNO₃)=0.1*85=8.5 г
Осталось NaOH: 0.75-0.2=0.55 моль
m(NaOH)=22г
Масса конечного раствора:
300 + m(NO₂)=300+ 0.2*46=309.2 г
Массовые доли:
w(NaOH)= 100*22/309.2=7.1%
w(NaNO₂) 100*6.9/309.2=2.2%
w(NaNO₂)= 100*8.5/309.2=2.7%
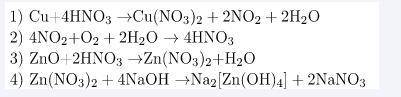
n(Ag)=21.6/108=0.2 mol
m(HNO3)=600*0.68=408g
n(HNO3)=408/63=6.5 mol азотка в избытке, считаем по серебру
n(NO2)= 0.2 моль
2NO2+ 2NaOH = NaNO2 + NaNO3 + H2O
m(NaOH)=300*0.1=30г
n(NaOH)=30/40=0.75 моль NaOH в избытке
n(NaNO2)=0.1 моль m(NaNO2)=0.1*69=6.9 г
n(NaNO3)=0.1 моль m(NaNO3)=0.1*85=8.5 г
осталось NaOH 0.75-0.2=0.55 моль m(NaOH)=22г
масса конечного раствора 300 + m(NO2)=300+ 0.2*46=309.2 г
массовые доли:
NaOH 100*22/309.2=7.1%
NaNO2 100*6.9/309.2=2.2%
NaNO3 100*8.5/309.2=2.7%