Составим уравнение реакции для эквивалента: 2C +S =X2S Масса серы в сульфиде =30-10.8 =19.2 Переведем в моль: Относительная атомная масса серы =32. Теперь разделим массу на молярную массу и найдем количество вещества: 19.2/32 =0.6 моль. Из реакции мы видим, что на 1 моль серы приходится 2 моль эквивалента. Таким образом разделим массу металла на количество вещества, чтобы найти молярную массу: 10.8/1.2 =9, однако этой массе соответствует бирилий, который не может иметь валентность 1. Теперь домножим молярную массу эквивалента на данную степень окисления: 9*3 =27 Таким образом неизвестный металл- это алюминий.
Сначала найдем массу спирта в растворе, умножив массу раствора на массовую долю компонента: 300*0.94 =288 г. Теперь переведем все данные вещества в моль. Чтобы найти количество вещества этилена разделим объем на молярный объем, а чтобы найти количество вещества спирта разделим массу на молярную массу: 4.12/22.4 =0.2 моль (этилена) 288/46 =6.2 ответы были округлены до десятых. Составим уравнение реакции гидротации этилена: C2H4 +H2O =C2H6O Таким образом из уравнения реакции мы видим, что на один моль этанола приходится 1 моль этилена, а значит их количества веществ, относятся также как масса и неизвестная масса. Составим пропорцию: 0.2/6.2 =4/X X =124 грамма технического карбида.
Объяснение:
m р-ра₁ = 100г
m р-ра₂ = 120г
ω₁ = 15% = 0,15
ω₂ = 8% = 0,08
ω₃ - ?
m в-ва₁ = m р-ра₁ × ω₁ = 100г × 0,15 = 15г
m в-ва₂ = m р-ра₂ × ω₂ = 120г × 0,08 = 9,6г
m в-ва₃ = m в-ва₁ + m в-ва₂ = 15г + 9.6г = 24.6г
m р-ра₃ = m р-ра₁ + m р-ра₂ = 100г + 120г = 220г
ω₃ =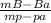 × 100% =
× 100% = 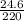 × 100% = 11,2%
× 100% = 11,2%