из 140г. азота можно получить 170г. аммиака
Объяснение:
Дано:
m(N₂)=140г.
m(NH₃)-?
1. Определим молярную массу азота и его количество вещества азота в 140г.:
M(N₂)=28г./моль
n₁(N₂)=m(N₂)÷M(N₂)=140г.÷28г./моль=5моль
2.Запишем уравнение реакции:
N₂+3H₂=2NH₃
по уравнению реакции:
n(N₂)=1моль n(NH₃)=2моль
по условию задачи:
n₁(N₂)=5моль n₁(NH₃)=10моль
3. Определим молярную массу аммиака и его массу количеством вещества 10моль:
M(NH₃)=17г./моль
m(NH₃)=n₁(NH₃)xM(NH₃)=10мольх17г./моль=170г.
4. ответ: из 140г. азота можно получить 170г. аммиака
Т.к всё органическое вещество должно быть 100% => щдесь имеется кислород. Вычисляем его массовую долю:
После того, как нашли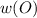 , нужно составить соотношение объёмной доли к атомной массе вещества, т.е.:
, нужно составить соотношение объёмной доли к атомной массе вещества, т.е.:
Затем делишь это всё на самое маленько число, которое у тебя получилось, т.е. 1,725 и получаешь отношение:
Получилось, что C - 3 атома, H - 6 атомов, O - 1 атом.
Т.к. здесь содержится всего лишь 1 атом O, то это или спирт, или альдегид, или кетон.
Но здесь нельзя составить ни спирт, ни кетон => остаётся альдегид. Составляем формулу: