При обработке соляной кислотой 27 г смеси двух металлов, проявляющих в соединениях валентность 2 и 3, выделилось 4 г газа. Атомная масса двух валентного металла в три раза меньше, чем атомная масса трех валентного, атомное отношение смеси соответственно равно 3:2. Определить какие металлы взяты. ??? если условие такое(когда оно полное), то вроде б так:
A+2HCl = ACl2+H2 2B+6HCl= 2BCl3 + 3H2 n(H2)=4/2 = 2 моль, пусть в первой реакции 2х моль, во второй Х моль; n(A)= 2 - X; n(B)= 2/3X Пусть молярная масса А=у, а молярная масса В=3у, тогда: (2-х)*у+2/(3х*3у) = 27 (2-х)/2/3х = 3/2 Х=1, у=9, это бериллий, второй металл - Алюминий
2,24 л
Объяснение:
Дано:
m(р-ра)=72 г
= 10%
Найти:
V-?
Формула соляной кислоты HCl
10% = 0,1
m(HCl)=m(р-ра)× ω/100 (пиши это дробью)=72×0,1=7,2 г
n(HCl)= = 7,2÷7,2=1 моль
= 7,2÷7,2=1 моль
V(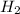 )=n(H2)×
)=n(H2)×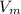 = 0,1×22,4=2,24 л
= 0,1×22,4=2,24 л
ответ: 2,24 л