ответ: ответ ниже. "⇒" и "=" заменить на стандартную "стрелочку" в химии.
Объяснение:
159) a)N( Степень окисления была -3, так как азот связан с тремя водородами, степень окисления которых равна +1) ⇒ N (степень окисления +2, так как связан с кислородом, степень окисления которого равна -2) ; Было -3, а стало +2, значит, N отдал 5 электрона.
б) O ( в 0 степени окисления, так как не связан больше ни с каким элементом) ⇒ O ( - 2 степень окисления, так как связан с двумя водородами, чья степень окисления равна +2) ; Было 0, а стало -2, значит, O получил 2 электрона.
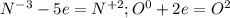 (1-(окисление азота) и (восстановление кислорода)
(1-(окисление азота) и (восстановление кислорода)
Там 5 электронов, а здесь 2 электрона. Приводим к наименьшему общему кратному, домножая первую часть уравнения на 2, а вторую - на 5. Получаем 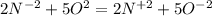 (К окислителю 2, к восстановителю 5) . В молекулярной форме это будет : 4NH3+5O2 ⇒ 4NO2 + 6H2O.
(К окислителю 2, к восстановителю 5) . В молекулярной форме это будет : 4NH3+5O2 ⇒ 4NO2 + 6H2O.
В 161 всё аналогично. Сразу перейду к коэффициентам
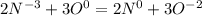 ,( к окислению идёт коэффициент 2, а к восстановителю 3), что в молекулярной формуле 4NH3+3O2⇒ 2N2 + 6 H2O
,( к окислению идёт коэффициент 2, а к восстановителю 3), что в молекулярной формуле 4NH3+3O2⇒ 2N2 + 6 H2O
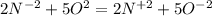
Карбонатная (временная) жесткость связана с присутствием в воде гидрокарбонатов кальция и магния, некарбонатная (постоянная) жесткость – хлоридов и сульфатов.
Общая жесткость воды рассматривается как сумма карбонатной и некарбонатной.
Удаление временной жесткости воды осуществляется путем осаждения из раствора ионов Ca2+ и Mg2+:
1) кипячением:
Сa(HCO3)2 = CaCO3↓ + CO2 + H2O;
Mg(HCO3)2 = MgCO3↓ + CO2 + H2O;
при кипячении соли разрушаются с образованием труднорастворимых карбонатов и ионы Ca2+ и Mg2+ удаляются из раствора.
2) добавлением гидроксида кальция (известкового молока):
Ca(HCO3)2 + Ca(OH)2 = 2CaCO3↓ + 2H2O;
3) добавлением соды:
Ca(HCO3)2 + Na2CO3 = CaCO3↓+ 2NaHCO3.
Удаление постоянной жесткости воды кипячением невозможно, поскольку хлориды и сульфаты магния и кальция не разрушаются, её можно удалить при добавлении соды или фосфата натрия:
CaSO4 + Na2CO3 = CaCO3↓ + Na2SO4;
MgCl2 + Na2CO3 = MgCO3↓ + 2NaCl;
3CaSO4 + 2Na3PO4 = Ca3(PO4)2 + 3Na2SO4.
Для удаления общей жесткости воды используют ионообменную смолу:
1) катионный обмен:
2RH + Ca2+ R2Ca + 2H+;
2) анионный обмен:
2ROH + SO42- R2SO4 + 2OH-
(где R – сложный органический радикал).
Ну там прочитай и подбери нужный ответ надеюсь