1-задание
m=n*M
a)40 г
б)31 г
в)22 г
Г)40 г
д)64 г
е)22 г
2-задание
a)Mg + H2SO4 = MgSO4 + H2↑
б)2Al + 3H2SO4(разб.) = Al2(SO4)3 + 3H2↑
в)2H3PO4(разб.) + 3Mg = Mg3(PO4)2↓ + 3H2↑
г)Ca + 2HCl(разб.) = CaCl2 + H2↑
д)_
е)Ag + 2HCl(газ)= 2AgCl + H2
ж)Fe + 2HCl(разб.) = FeCl2 + H2↑
з)Fe2O3 + 6HCl(газ) = 2FeCl3 + 3H2O
и)Hg + 2H2SO4(конц.) = HgSO4 + SO2↑ + H2O
к)_
л)MgCl2 + H2O(пар) = MgO + HCl
м)CaO + 2HCl(разб.) = CaCl2 + H2O
н)_
о)3H2SO4 + 2Fe(OH)3 = Fe2(SO4)3 + 6H2O
п)Cu + H2SO4(конц., хол.) = CuO + SO2 + H2O
р)CuO + H2SO4 = CuSO4 + H2O
3-задание
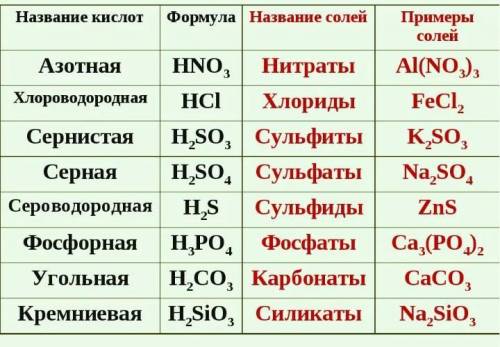
H2SO4 - SO3
H2SO3 - SO2
HNO3 - NO2
HNO2 - N2O3
H3PO4 - P2O5
H2CO3 - CO2
H2SiO3 - SIO2
1Соли сернистой кислоты называются сульфитами. Как кислота двухосновная, она образует соли двух типов, например; NaHS03 - бисульфит натрия и Na2S03 - сульфит натрия.. Соли сернистой кислоты , образованные катионами сильных оснований, в водных растворах имеют щелочную реакцию.
3 Гидролиз солей — это химическое взаимодействие ионов соли с ионами воды, приводящее к образованию слабого электролита -кислоты (или кислой соли), или основания (или основной соли). Слово «гидролиз» означает разложение водой («гидро»-вода, «лизис» — разложение)


1) 50г + 50г =100г
2)50*5/100=2,5г
3)50*5/100=2,5г
4)2,5+2,5=5г
5)5г делим на 100г = 1/20
ответ:1/20