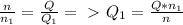
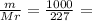 4,4 моль
4,4 моль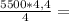 6,050 кДЖ
6,050 кДЖ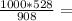 581,5г
581,5г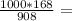 185г
185г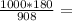 198,25г
198,25г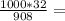 35,25г
35,25г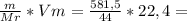 296л
296л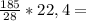 148л
148л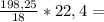 246,7л
246,7л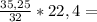 24,675л
24,675лТо есть концентрация полученного раствора должна стать: 15 + 5 = 20%
1) Если концентрацию раствора выразить в долях единицы, то массу растворенного вещества в граммах находят по формуле:
m(в-во) = ω * m(p-p)
где: m(p-p) - масса раствора в граммах, ω - массовая доля растворенного вещества, выраженная в долях единицы .
15% - это 0,15 в долях единицы, а 20% - 0,2
2) Обозначим массу раствора после упаривания через Х граммов. Так как при упаривании масса растворенного вещества не изменяется, то можем записать:
0,18 · 800 = 0,2 · Х
0,2Х = 120
Х = 600
3) То есть масса раствора была 800 г, а стала 200 г. Значит количество выпаренной воды равно:
800 - 600 = 200 г
ответ: 200 г воды
1) n(CO2)=8,8/44=0,2моль
n(H2O)=3,6/18=0,2моль
n(C)=0,2моль
n(H)=0,2*2=0,4моль
2)Проверим содержит ли он кислород:
m(C)+m(H)=0,2*12+0,4*1=2,8г
m(C)+m(O)=m(x), значит этот углеводород не содержит кислорода.
3)Найдем отношение:
n(C):n(H)=0,2:0,4(разделим на меньшее число)
n(C)=n(H)=1:2
Простейшая ф-ла этого угл-да CH2
4)Найдем молекулярную формулу:
M(CH2)=14г/моль
M(вещ-ва)=0,875*32=28г/моль
Значит изначальные цифры увел. в 2 раза
Молекулярная формула вещ-ва будет такова: C2H4(этилен)