Дано
m(Na)=2,3г.
m(C₂H₅OH)=5г.
Vm=22,4л./моль
V(H₂)-?
1. Определим молярную массу натрия и его количество вещества в 2,3г.:
M(Na)=23г./моль
n₁(Na)=m(Na)÷M(Na)=2,3г.÷23л./моль=0,1моль
2. Определим молярную массу этилового спирта и его количество вещества в 5г.:
M(C₂H₅OH)=)=12x2+5+16+1=46г./моль
n₁(C₂H₅OH)=m(C₂H₅OH)÷M(C₂H₅OH)=5г.÷46г./моль=0,1моль
3. 2C₂H₅OH +2Na=2C₂H₅ONa+H₂
по уравнению реакции:
n(Na)=2моль n(C₂H₅OH)=2моль
по условию задачи:
n₁(Na)=0,1моль n₁(C₂H₅OH)=0,1моль
Количества вещества натрия и этилового спирта равны, поэтому для решения задачи можно можна брать или натрий или этиловый спирт:
по уравнению реакции:
n(Na)=2моль n(₂H)=1моль
по условию задачи:
n₁(Na)=0,1моль n₁(H₂)=0,05моль
4. Определим объем образовавшегося водорода:
V(H₂)=n₁(H₂)xVm
V(H₂)=0,05мольх22,4л./моль=1,12л.
5. ответ: если для реакции взяты 2,3г. натрия и 5г. этилового спирта, то образуется 1,12л. водорода.
1. Напишем реакции в общем виде.
CnH2n-2 + 2H₂ = CnH2n+2.
CnH2n+2 + Cl₂ = CnH2n-1Cl + HCl.
2. По уравнениям реакций мы видим, что количество вещества (моль) CnH2n-2 равно количеству вещества CnH2n-1Cl, значит мы можем сделать пропорцию.
m (CnH2n-2) ÷ M (CnH2n-2) = m (CnH2n-1Cl) ÷ M (CnH2n-1Cl). Подставим все значения в эту пропорцию и сделаем уравнение.

3. Переносим это всё в левую сторону, подводим две дроби к общему знаменателю, домножаем числители, приравниваем всё это дело к нулю.
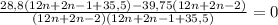
4. Знаменатель можно откинуть, с ним мы не работаем. Написала для наглядности, чтобы было понятно, как я решала. Далее решаем по правилу: дробь равна нулю, когда числитель равен нулю.
28,8(12n+2n-1+35,5)-39,75(12n+2n-2) = 0
Не буду расписывать всё решение, потому что это химия, а не алгебра.
В общем, в итоге у нас получается n = 7.
Таким образом, формула исходного углеводорода — C₇H₁₂, атомов водорода в нём = 12.
ответ: 12.
a) Атомная сила это опасно поиграй в Stalker
б) Хз
в) была в майами?
Объяснение:
Нема