Дано :
ω(вещества) = 30% = 0,3.
m(вещества) = 20 г.
Найти :
m(раствора) = ?
Массовая доля растворённого вещества - это отношение массы растворённого вещества к массе всего раствора.Обозначим массу растворителя за х.
Тогда m(раствора) = m(вещества) + m(растворителя) = 20 г + х.
Составим уравнение на основании определения массовой доли растворённого вещества -
0,3 = 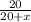
0,3*(20 + х) = 20
20 + х = 20 : 0,3
20 + х = 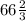 г - масса всего раствора.
г - масса всего раствора.
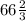 г.
г.
1000 моль х моль
СaCO3 = CaO + CO2 (газ, стрелка вверх)
1 моль 1 моль
n = m/M
M(CaCO3) = 40 + 12 + 16*3 = 100 г/моль
100 кг = 100 000 г
100 000 г - это 100 %
х г - это 20 %
х = 20 000 (г) = > это столько г примесей => m чист(CaCO3) = 100 000 г - 20 000 г = 80 000 г
n(CaCO3) = 80 000 г / 100 г/моль = 800 моль
n(CaCO3) = n(CaO) = 800 моль
800 моль х моль
CaO + H2O = Ca(OH)2
1 моль 1 моль
n(CaO) = n(Ca(OH)2) = 800 моль
Но выход продукта составляет 80 % от теоретически возможного, то есть 80 % от 800 моль
800 моль - это 100%
х моль - это 80%
х = 640 => n(Ca(OH)2) = 640 моль
Масса раствора — 300 г, что составляет 100%. Массовая доля вещества нам известна — 20%, массовая доля воды равна 100%-20%=80%. Теперь приступим к расчетам. Нам нужно поочередно умножить массу раствора на массовые доли в-ва и воды. 300 г * 0,2 = 60 г. — масса вещества 300 г * 0,8 = 240 г. — масса воды ответ: 60 г; 240 г.
Объяснение: