
▶Качественной реакцией на сульфит-ионы 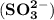 является выделение бесцветного газа с резким запахом - оксида серы (Ⅳ)
является выделение бесцветного газа с резким запахом - оксида серы (Ⅳ) 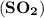 при добавлении в раствор сильной кислоты (например,
при добавлении в раствор сильной кислоты (например, 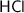 ).
).
 - молекулярное уравнение.
- молекулярное уравнение.
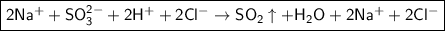 - полное ионное уравнение.
- полное ионное уравнение.
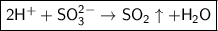 - сокращённое ионное уравнение.
- сокращённое ионное уравнение.
▷Признак реакции - выделение бесцветного газа с резким запахом - 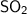 .
.
Качественной реакцией на сульфид-ионы 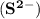 является выделение бесцветного газа с неприятным запахом - сероводорода
является выделение бесцветного газа с неприятным запахом - сероводорода 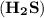 при добавлении в раствор сильной кислоты (например,
при добавлении в раствор сильной кислоты (например, 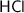 ).
).
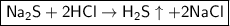 - молекулярное уравнение.
- молекулярное уравнение.
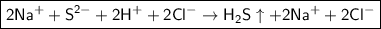 - полное ионное уравнение.
- полное ионное уравнение.
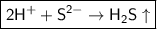 - сокращённое ионное уравнение.
- сокращённое ионное уравнение.
▷Признак реакции - выделение бесцветного газа с неприятным запахом - 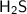 .
.
Итак, если при добавлении соляной кислоты в одну из пробирок выделяется газ с запахом жжённых спичек - 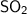 , то это значит, что в растворе содержится сульфит натрия -
, то это значит, что в растворе содержится сульфит натрия - 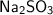 . Если при добавлении соляной кислоты в одну из пробирок выделяется газ с запахом тухлых яиц -
. Если при добавлении соляной кислоты в одну из пробирок выделяется газ с запахом тухлых яиц - 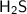 , то это значит, что в растворе содержится сульфид натрия -
, то это значит, что в растворе содержится сульфид натрия - 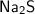 .
.
1. Составим уравнение реакции:
4Al + 3O2 = 2Al2O3;
2. определяем химические количества алюминия, оксида алюминия и вступающего в реакцию кислорода:
n (Al) = m (Al) : M (Al) = 5,4 : 27 = 0,2 моль;
n (Al2O3) = n (A) : 2 = 0,2 : 2 = 0,1 моль;
n (O2) = n (Al) * 3 : 4 = 0,2 * 3 : 4 = 0,15 моль;
3. рассчитываем массы:
m (Al2O3) = n (Al2O3) * M (Al2O3);
M (Al2O3) = 2 * 27 + 3 * 16 = 102 г/моль;
m (Al2O3) = 0,1 * 102 = 10,2 г;
m (O2) = n (O2) * M (O2) = 0,15 * 32 = 4,8 г.
ответ: 10,2 г Al2O3 содержит 4,8 г кислорода.
ZnO+HNO3=Zn(NO3)2+H2O
ZnO + 2H⁺ + 2NO3⁻ = Zn²⁺ + 2 NO3⁻ + H2O
ZnO + 2H⁺ = Zn²⁺ + H2O
2Al + 3H2SO4 (р.) =Al2(SO4)3 + 3 H2↑
6H⁺+3SO4²⁻ +2Al = 2Al³⁺ +3SO4²⁻+3H2↑
6H⁺+2Al⁰⇒2Al³⁺+3H2⁰↑
HNO3 + CuSO4 = nein
2HCL + FeS = FeCl2+ H2S
2H⁺ + 2CL⁻ + FeS = H2S + Fe²⁺ + 2CL⁻
2H⁺ + FeS = H2S + Fe²⁺
3H2SO4 + 2Fe(OH)3 = Fe2(SO4)3+ 6H2O
6H⁺ + 3SO4²⁻ + 2Fe(OH)3 = 2Fe³⁺ + 3SO4²⁻ +6H2O
6H⁺ + 2Fe(OH)3 = 2Fe³⁺ + 6H2O