Уравнение реакции( один из вариантов):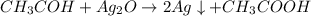
Чтобы расчитать выход продукта, нам нужно узнать сколько теоретически должно было выделиться продукта( "на бумаге").
Воспользуемся известной массой уксусного альдегида и найдём, сколько этого самого альдегида вступило в реакцию:
n( количество вещества) = m( масса) / M( молярная масса) - общая формула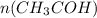 = 4,4 / 44= 0,1 моль
= 4,4 / 44= 0,1 моль
Из уравнения реакции видно, что коэффициент перед уксусным альдегидом равен коэффициенту перед уксусной кислотой, т.е. 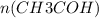 =
= 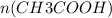 = 0,1 моль
= 0,1 моль
Теперь, пользуясь уже знакомой формулой n( количество вещества) = m( масса) / M( молярная масса), мы можем найти массу ( теоретическую) уксусной кислоты: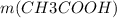 =
= 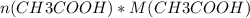 = 0,1 * 60 = 6 г.
= 0,1 * 60 = 6 г.
Выход продукта расчитываем по формуле:
w = m( практ) / m( теор) * 100% = 90%
ответ: выход продукта составил 90%.
112г хл
Fe + 2HCI = FeCI2 + H2
v=1моль v=1моль
М=56г/моль Vm=22,4л/моль
m=56г V=22,4л
сост.пропорцию:
112г/56г=хл/22,4л
х=(22,4л*112г)/56г=44,8л
отв.:44,8л водорода
хг 180г
2Fe(OH)3 = Fe2O3 + 3H2O
v=2моль v=1моль
М=107г/моль М=160г/моль
m=214г m=160г
сост.пропорцию:
хг/214г=180г/160г
х=(214г*180г)/160г=240,75г
отв.:240,75г гидроксида железа 3