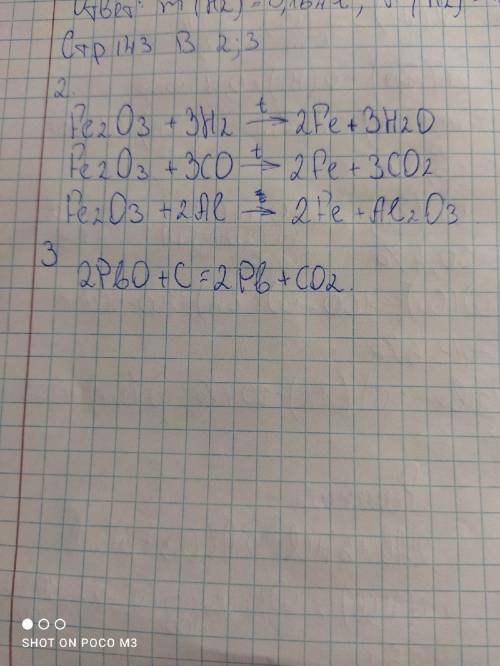
6) щелочи: NaOH, KOH, LiOH,Ca(OH)2
нерастворимые: Ti(OH)3, Mg(OH)2
9) KOH + HNO3= H2O + KNO3
n=m÷M
n(HNO3) = 18,9÷63= 0,3 моль
по уравнению следует, что: n(HNO3)= n(KNO3)=0,3 моль
m=n×M
m(KNO3) = 0,3 × 101= 30,3 г
ответ:30,3г
10) из дано этот элемент щелочноземельный металл, все ЩЗМ реагируют с азотом одинаково(азот восстанавливается до -3), примем щзм за Х:
3X+N2=X3N2
n= V÷Vm
(для газов при н.у. Vm=22,4 л/моль)
n(N2) = 1,12:22,4= 0,05 моль
по уравнению реакции: 3×n(N2)= n(X)
n(X)= 0,05×3= 0,15 моль
M=m÷n
M(X)=3,6÷0,15=24г/моль => Х - это Мg
схема электронного строения на фото
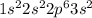
Объяснение:
CO2 + Ca(OH)2 = H2O + CaCO3
Ca2+ + 2OH− + CO2 = CaCO3 + H2O
CaCO3 + 2HNO3 = CO2↑ + H2O + Ca(NO3)2
Полнаяформа:2H+ + 2NO3- + CaCO3 = Ca2+ + 2NO3- + H2O + CO2
Краткаяформа:2H+ + CaCO3 = Ca2+ + H2O + CO2
H2O + CO2 + CaCO3(тверд.) = Ca(HCO3)2(разб.)
CO2 + Ca(OH)2 = H2O + CaCO3
Ca2+ + 2OH− + CO2 = CaCO3 + H2O
H2O + CO2 + CaCO3(тверд.) = Ca(HCO3)2(разб.)
CO2 + Ca(OH)2 = H2O + CaCO3
Ca2+ + 2OH− + CO2 = CaCO3 + H2O
H2O + CO2 + CaCO3(тверд.) = Ca(HCO3)2(разб.)
H2O + CO2 + CaCO3(тверд.) = Ca(HCO3)2(разб.)
CaCO3 + 2HNO3 = CO2↑ + H2O + Ca(NO3)2
Полнаяформа:
2H+ + 2NO3− + CaCO3 = Ca2+ + 2NO3− + H2O + CO2
Краткаяформа:
2H+ + CaCO3 = Ca2+ + H2O + CO2
CaCO3 + H2[SiF6] = H2O + CO2↑ + Ca[SiF6]↓
2H+ + [SiF6]2− + Ca2+ + CO32− = Ca[SiF6]↓ + CO2↑ + H2O
Объяснение:
привет :з
для того, чтобы расставлять коэффициенты при метода электронного баланса, следует знать несколько правил и уметь правильно расставлять степени окисления.
Какие должны быть знания относительного самого метода:
например, Fe (+3) говорит о том, что у железа не хватает 3 электрона, если O (-2), то у него в избытке 2 электрона; у отдельно стоящих элементов (например, Н2) степень окисления равна 0, это говорит о том, что электроны в достатке.
окислитель - тот, кто принимает электроны, восстановитель - тот, кто отдаёт. окисление - отдача электронов, восстановление - принятие электронов.
Алгоритм расстановки:
1. Сначала расставляем степени окисления над элементами;
2. Ищем те, у кого меняются степени окисления слева направо;
3. Дальше используем знания, которые я написала выше (+ не хватает, - в избытке, 0 достаточно);
4. Ищем общее кратное и делим на количество электронов;
5. Расставляем коэффициенты в уравнении рядом с теми элементами, у которых общее кратное разделили на количество электронов.
(Примечание: в данном случае у железа можно и обычным поставить коэффициент, поэтому методом электронного баланса не стала)