В пробирке 1 находится HBr - кислота. В пробирке 2 находится NH4Br - слабое основание.
Водород в своем составе имеют кислые, комплексные соли и кислоты, но для кислых и комплексных необходимо не менее трех веществ, так что в первой пробирке находится исключительно кислота.
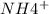 - катион аммония, единственное соединение неметалла с водородом, на ряду с фосфонием
- катион аммония, единственное соединение неметалла с водородом, на ряду с фосфонием 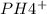 , которое проявляет слабые металлические свойства, то есть играет роль восстановителя в соединениях с неметаллами, а как мы знаем, подобные неорганические соединения относятся к классу солей.
, которое проявляет слабые металлические свойства, то есть играет роль восстановителя в соединениях с неметаллами, а как мы знаем, подобные неорганические соединения относятся к классу солей.
ну для всех это ты загнул тут математические издевательства над химиками
А) 4Fe(т) + 3О2(г) = 2Fe2O3(т)
dH это будет дельта Н если что
dHреак = сумма dH продуктов - сумма dH до реакции
dH(Fe) = dH(O) = 0
dH(Fe2O3) = -822.2
dHреак = 2*(-822.2) - (0 + 0) = 2 * (-822.2) = -1644,4
dS это изменение энтропии
dS(Fe) = 27.2
dS(O2) = 205
dS(Fe2O3) = 90
dSреак = 2 * 90 - (4 * 27.2 + 3 * 205) = 180 - 723.8 = -543.8
Так как знак изменения энтропии и выделения энергии одинаковы, то реакция оборотна
изменение энергии гиббса - dG
dG = dH - T * dS
dG = -1644.4 - 298.15 * (-0.5438) = -1644.4 + 162.13 = -1482.26
изменение энергии гиббса меньше нуля, значит реакция при стандартных условиях может самопроизвольно протекать