ответ: Это цинк с молекулярной массой 65 г/моль. Осталось непрореагировавшей 1,95 грамм серной кислоты.
Объяснение:
Ме+Н2SO4=> MeSO4+H2
При взаимодействии металла с кислотой выделилось 0,45 литра водорода, что составляет 0,45/22,4=0,02 моль газа. В реакцию в соответствии с уравнением также вступило 0,02 моль металла, соответственно его молекулярная масса составляет 1,3/0,02=65 грамм/моль, что соответствует молекулярной массе цинка.
В реакцию вступило также 0,02 моль серной кислоты, а в исходном растворе её было 3,9/98=0,04 моль. Соответственно, 0,02 моль серной кислоты осталось непрореагировавшей, что составляет половину от исходной массы, а именно 1,95 грамм.
Как-то так
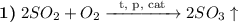
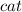 - катализатор (кат). Например:
- катализатор (кат). Например: 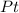 , или
, или 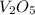 , или
, или 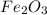 .
.

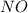 - оксид азота (II) / монооксид азота / окись азота
- оксид азота (II) / монооксид азота / окись азота
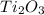 - оксид титана (III) / трЁхокись титана
- оксид титана (III) / трЁхокись титана
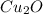 - оксид меди (I) / оксид димеди / закись меди / гемиоксид меди / куприт
- оксид меди (I) / оксид димеди / закись меди / гемиоксид меди / куприт
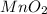 - оксид марганца (IV) / диоксид марганца / пиролюзит
- оксид марганца (IV) / диоксид марганца / пиролюзит
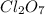 - оксид хлора (VII) / дихлоргептаоксид / хлорный ангидрид
- оксид хлора (VII) / дихлоргептаоксид / хлорный ангидрид
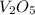 - оксид ванадия (V) / пентаоксид диванадия
- оксид ванадия (V) / пентаоксид диванадия
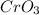 - оксид хрома (VI) / триоксид хрома / трЁхокись хрома / хромовый ангидрид
- оксид хрома (VI) / триоксид хрома / трЁхокись хрома / хромовый ангидрид
*Выбирай, что нравится. Все наименования, написанные первыми - систематические, т.е. используются на "официальном" уровне, среди химиков, международная - лично я писал бы их.
Номер 3.а) 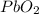
б) 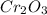
в) 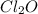
г) 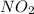
д) 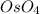
3I 2J(-)-2e->J2(0) восстановитель окисление
2I Cr(+6)+3e->Cr(3+) окислитель восстановление
2) 5H2O2+2KMnO4+3H2SO4=5O2+K2SO4+2MnSO4+8H2O
5I 2O(-2)-4e->O2(0) восстановитель окисление
4I Mn(7+)+5e->Mn(2+) окислитель восстановление
3) 2NaNO2+2NaJ+2H2SO4=2NO+J2+2Na2SO4+2H2O
2I N(3+)+1e->N(2+) окислитель, восстановление
1I 2J(-)-2e->J2(0) восстановитель, окисление
4) KBrO3+5KBr+3H2SO4=3K2SO4+3Br2+3H2O
1I Br(5+)+10e->Br2(0) окислитель восстановление
5I 2Br(-)-2e->Br2(0) восстановление окислитель