Согласно условию задачи n(Na2SO4) : n(Ba(OH)2) = 1 : 3, n(атомы соли и щелочи) = 1 моль.
Пусть n(Na2SO4) = x моль, тогда n(атомы соли) = 7х, n(Ba(OH)2) = 3x моль, n(атомы щелочи) = 5*3х = 15x.
Так как n(атомов соли и щелочи) = 1 моль, то 7x + 15x = 1,
x = 1/22 = 0,0455 моль, n(Na2SO4) =0,0455 моль; n(Ba(OH)2) = 0,136 моль.
Na2SO4 + Ba(OH)2 = ↓BaSO4 + 2NaOH
0,0455 0,136 (по условию задачи)
Гидроксид бария взят в избытке, сульфат натрия прореагирует полностью.
В реакцию вступят по 0,0455 моль сульфата натрия и гидроксида бария, образуются 0,0455 моль сульфата бария (нерастворимого в воде) и 2*0,0455 = 0,091 моль гидроксида натрия. Также в растворе останется неизрасходованный гидроксид бария в количестве 0,136 – 0,0455 = 0,091 моль.
Масса жидкости над осадком будет равна массе исходных веществ за вычетом осадка (сульфата бария):
m(жидкости) = m(исходный Na2SO4) + m(исходный Ba(OH)2) + m(H2O) – m(осадок, BaSO4) = 0,0455*142 + 0,136*171 + 200 – 0,0455*233 = 219 г.
ответ: 219 граммов
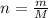 , где m - масса вещества, а M - его [вещества] молярная масса.
, где m - масса вещества, а M - его [вещества] молярная масса. 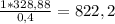
4Al (порошок)+ 3O2 → 2Al2O3
Al2O3 + 6HCl (конц. горячий р-р)→ 2AlCl3 + 3H2O
AlCl3 + 3NaOH (разб. р-р)→ Al(OH)3 + 3NaCl
2Al(OH)3 → Al2O3 + 3H2O
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Объяснение: